题目内容
【题目】某化学兴趣小组设计了一组“吹气球”实验,三套装置如下图:
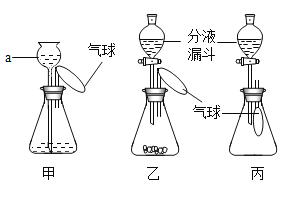
(1)甲装置:
①仪器![]() 的名称为_____________;
的名称为_____________;
②向![]() 中加水会看到气球胀大,一段时间内气球大小没有变化,说明该装置气密性___________
中加水会看到气球胀大,一段时间内气球大小没有变化,说明该装置气密性___________
(2)乙装置:
①若生成![]() 使气球胀大,则锥形瓶中所装的固体物质可以是__________;反应的方程式为:____________
使气球胀大,则锥形瓶中所装的固体物质可以是__________;反应的方程式为:____________
②若生成![]() 使气球胀大,则反应的化学方程式为___________
使气球胀大,则反应的化学方程式为___________
③若锥形瓶中装有![]() 固体,分液漏斗中加入少量水,则气球胀大的主要原因是_________
固体,分液漏斗中加入少量水,则气球胀大的主要原因是_________
(3)丙装置:若锥形瓶中盛满![]() ,欲使气球胀大,则分液漏斗中的液体可以是_____________
,欲使气球胀大,则分液漏斗中的液体可以是_____________
【答案】长颈漏斗 良好 二氧化锰 2H2O2![]() 2H2O+O2↑ Zn+H2SO4=ZnSO4+H2↑ NaOH固体溶于水放热,装置内气压增大,气球胀大 氢氧化钠溶液
2H2O+O2↑ Zn+H2SO4=ZnSO4+H2↑ NaOH固体溶于水放热,装置内气压增大,气球胀大 氢氧化钠溶液
【解析】
(1)①仪器a的名称为长颈漏斗;
②向a中加水会看到气球胀大,一段时间内气球大小没有变化,说明该装置气密性良好。
故填:①长颈漏斗;②良好;
(2)①该装置是固、液在常温下制取气体的装置,若生成O2使气球胀大,则锥形瓶中所装的固体物质可以是催化剂二氧化锰,倒入的液体是过氧化氢溶液,反应的方程式为;2H2O2![]() 2H2O+O2↑;故填:二氧化锰;2H2O2
2H2O+O2↑;故填:二氧化锰;2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
②锌和稀硫酸反应生成硫酸锌和氢气,反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑。故填:Zn+H2SO4=ZnSO4+H2↑;
③氢氧化钠溶于水放出大量的热,装置内气压增大,气球胀大。故填:NaOH固体溶于水放热,装置内气压增大,气球胀大;
(3)丙中CO2气体被吸收时,装置内压强减小,内部的气球就会胀大,氢氧化钠溶液可吸收二氧化碳气体。故填:氢氧化钠溶液。

【题目】实验室中氯酸钾样品含有杂质,为了测定样品中氯酸钾的质量分数,取 10g 该样品与 1g 二氧化锰混合加热 t1 时间后(假设杂质不参加反应),冷却,称量剩余固体质量,重复以上操作,依次称得加热 t2、t3、t4 时间后剩余固体的质量,记录数据如下表:
加热时间 | t1 | t2 | t3 | t4 |
剩余固体质量/g | 10.04 | 9.08 | 8.12 | 8.12 |
(1)请问完全反应后产生氧气的质量为_____g 。
(2)求该样品中氯酸钾的质量分数_____(要求写出计算过程)。反应的化学方程式为:2KClO3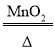 2KCl+ 3O2↑
2KCl+ 3O2↑
【题目】人类生活离不开化学,下列对某一主题知识归纳都正确的是( )
A安全知识 | B生活常识 |
图书档案着火—用水灭火 “干冰”灭火原理—降低可燃物的着火点 用铁矿石炼铁尾气要净化处理— | 除去水中色素和异味—活性炭 常用作食品干燥剂—熟石灰 用洗涤剂去油污—溶解作用 |
C物质的微粒观 | D物质的鉴别和除杂 |
碘酒是混合物—组成中的分子种类不同 稀硫酸能导电—溶液中有自由移动的离子 温度计测体温时汞柱升高—汞原子体积增大 | 鉴别 鉴别聚乙烯和聚氯乙烯—灼烧闻气味 除去碳酸钙粉末中的碳酸钠—用水 |
A.AB.BC.CD.D
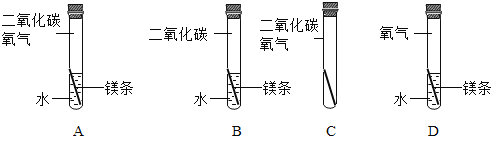
【题目】小明为验证质量守恒定律,做了镁粉在空气中燃烧的实验(如图1),该反应的化学力程式是______。实验结束,他发现镁粉在空气中充分燃烧后,产物中还有少量黄色固体。为了弄清黄色固体的成分,小明进行了如下实验探究:
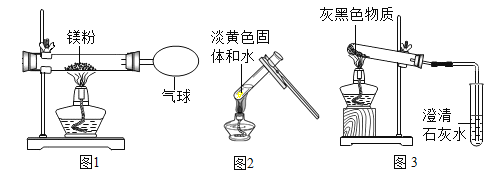
(查阅资料)
①镁能与氮气剧烈反应生成黄色的氮化镁(![]() )固体。
)固体。
②氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
(设计实验)小明用图2所示的实验(部分操作没有画出),验证黄色固体为![]() ,请完成下列实验报告。
,请完成下列实验报告。
操作步骤 | 实验现象 | 实验结论 |
取少量黄色固体于试管中,加入适量水,加热,并将湿润的红色石蕊试纸放在试管口 | _______ | 黄色固体为 |
(交流与思考)小明发现久置的镁条上有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?他叫来了小亮、小红一起进行了实验探究:
(猜想)小明认为可能是![]() ;
;
小亮认为可能是![]() ;
;
小红认为可能是![]() 。
。
小红认为小明的猜想是错误的,其理由是___________。
(查阅资料2)①![]() 受热分解产生两种氧化物。
受热分解产生两种氧化物。
②![]() 受热分解产生三种氧化物。
受热分解产生三种氧化物。
(实验探究)小亮进行实验(见图3),发现试管口有液滴出现,澄清石灰水变浑浊,同时试管内生成白色固体。
(实验分析)实验后,小亮认为小红的猜想也是错误的,其理由是___________。
(实验反思)要验证小亮的猜想,实际上只需证明灰黑色“外衣”的形成是否需要二氧化碳即可。为了证明这一猜想,需要进行如图所示实验中的___________(填序号,下同)和___________。