题目内容
【题目】某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
(提出问题)氧化铜是否也能作氯酸钾分解的催化剂?
(设计并完成实验)
Ⅰ.将3.0g氯酸钾放在试管中加热
Ⅱ.将3.0g氯酸钾与1.0g二氧化锰均匀混合加热
Ⅲ.将xg氯酸钾与1.0g氧化铜均匀混合加热
(实验现象分析)Ⅲ中x的值应为_____,将实验Ⅰ和Ⅲ比较可证明_____,将实验Ⅲ反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到1.0g黑色粉末,再将黑色粉末和xg氯酸钾混合加热,现象与实验Ⅲ相同,此步骤是为了证明氧化铜在该化学反应前后_____和_____都不变。
(结论1)氧化铜也能作氯酸钾分解的催化剂,请写出实验Ⅲ中的化学反应文字表达式_____。
(继续探究)小组同学完成上述实验后,又深一步进行“氧化铜用量与一定质量氯酸钾
制取氧气反应速率关系”的探究,下表是他们的有关实验数据,请你回答有关问题:
氧化铜与氯酸钾的质量比 | 1/40 | 1/20 | 1/10 | 1/5 | 1/3 | 1/2 | 2/3 | 1/1 | 2/1 |
生成1L氧气所需的时间(s) | 124 | 79 | 50 | 54 | 75 | 93 | 106 | 153 | 240 |
(分析整理)据上表可知氧化铜用量过多,产生氧气的速率_____(填“变快”、“变慢”或“不变”),氧化铜与氯酸钾的质量比为_____时,反应速率最快。
(结论2)在化学反应中催化剂的用量_____(填“是”或“不是”)越多越好。
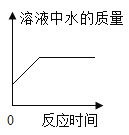
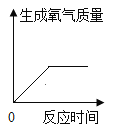
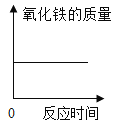
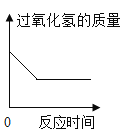
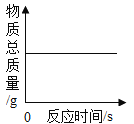
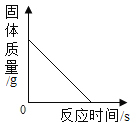
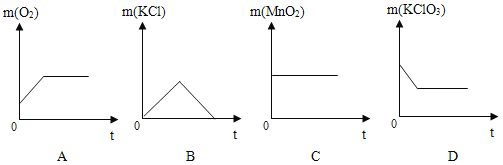
(能力提升)在一定质量的氯酸钾中加入少量的氧化铜并加热到不再产生气体为止,下图中能正确表示反应前后各物质的质量变化(m)与时间(t)关系的是_____。
(提出问题)②双氧水分解速度还和什么因素有关。
(设计并完成实验)
双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生产生O2体积 | |
Ⅰ | 50.0g | 1% | 0.1g | 9mL |
Ⅱ | 50.0g | 2% | 0.1g | 16mL |
Ⅲ | 50.0g | 4% | 0.1g | 31mL |
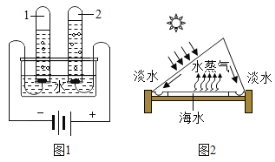
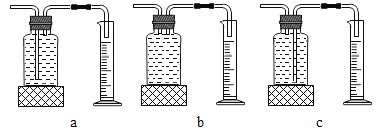
本实验中,测量O2体积的装置是_____(填编号)。
(结论3)在相同条件下,双氧水的_____,双氧水分解得越快。
【答案】3.0 CuO能否改变KClO3分解的速率 质量 化学性质 氯酸钾![]() 氯化钾+氧气 变慢 1:10 不是 C c 浓度越大
氯化钾+氧气 变慢 1:10 不是 C c 浓度越大
【解析】
[实验现象分析]由控制变量法的思想可知,x为3.0;根据催化剂能改变化学反应的速率,将实验Ⅰ和Ⅲ比较可证明CuO能否改变KClO3分解的速率,将实验Ⅲ反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到1.0g黑色粉末,再将黑色粉末和xg氯酸钾混合加热,现象与实验Ⅲ相同,此步骤是为了证明氧化铜在该化学反应前后的质量和化学性质都不变。故填:3.0;CuO能否改变KClO3分解的速率;质量;化学性质;
[结论1]氯酸钾在二氧化锰作催化剂加热的条件下分解为氯化钾和氧气;故填:氯酸钾![]() 氯化钾+氧气。
氯化钾+氧气。
[分析整理]根据实验数据可知氧化铜用量过多,产生氧气的速率变慢,而当氧化铜与氯酸钾的质量比为1:10时,反应速率最快;故填:变慢;1:10;
[结论2]根据实验数据分析可知在化学反应中催化剂的用量不是越多越好;故填:不是;
[能力提升]在一定质量的氯酸钾中加入少量的氧化铜并加热到不再产生气体为止,开始没有氧气,A错误,氯化钾的质量从0增大到不变,不会变无,B错误;
氧化铜是该反应的催化剂,质量不变,C正确;
加热到不再产生气体,则氯酸钾的质量为0,D错误;故填:C;
[设计并完成实验]气体短管进长管出才能排出试剂瓶中的水,所以应该选择c装置作为实验装置;故填:c;
[结论]从表中实验数据可知双氧水浓度越大,分解得越快。故填:浓度越大

【题目】氧气能跟很多物质反应。根据如图所示实验,并阅读资料,回答下列问题。
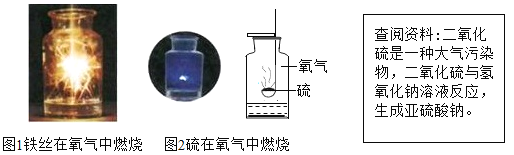
Ⅰ小明对图1铁丝在氧气中燃烧为什么会火星四射进行探究。下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录.请你分析回答:
物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
燃烧时的现象 | 剧烈燃烧,发出耀眼白光,无火星 | 剧烈燃烧极少火星 | 剧烈燃烧少量火星 | 未填 |
①表中“未填”部分的内容应为__________________;
②铁丝在氧气燃烧的文字表达式是______________________。
③通过以上探究,你认为铁丝燃烧产生火星四射现象的原因可能是__________。
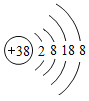
Ⅱ图2中反应的文字表达式为______________,集气瓶中加入的液体可能是____________。
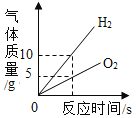
【题目】下列图象能正确反映对应关系的是( )
|
|
|
|
A.用等质量、等浓度的过氧化氢溶液制取氧气 | B.将水通电一段时间 | C.一定质量的红磷在密闭容器中燃烧 | D.加热一定质量的氯酸钾制氧气 |
A. A B. B C. C D. D