题目内容
【题目】如图所示为实验室中常见的气体制备和收集装置.请回答下列问题:
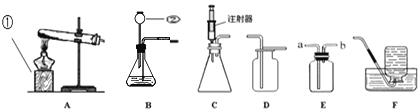
(1)写出图中仪器②的名称: _____________.
(2)实验室用氯酸钾制取一瓶纯净的氧气,应选用发生装置和收集装置是________(填字母序号),反应的化学方程式为______________![]()
(3)用D收集一瓶氧气,验满的方法是_________________![]()
(4)欲想用装置E排水集气法来收集一瓶氧气用于实验,则气体应该从_____________![]() (填“a”或“b”)端通入
(填“a”或“b”)端通入
(5)小明同学发现装置B有一处明显错误,请帮他指出来:_________________。
【答案】长颈漏斗 A和F 化学方程式略 用带火星的小木条放在集气瓶瓶口,小木条复燃,证明已满 b 长颈漏斗下端没有伸入液面以下或锥形瓶中导管太长(伸入液面以下了)
【解析】
(1)仪器②是长颈漏斗,故填:长颈漏斗;
(2)实验室用氯酸钾制取氧气,是固体加热型反应,故发生装置是A,氧气不易溶于水,可以用排水法收集,氧气的密度大于空气,可以用向上排空气法收集,但用排水法收集的气体较为纯净;氯酸钾在二氧化锰的催化下加热生成氯化钾和氧气;故填:AF;2KClO3![]() 2KCl+3O2↑;
2KCl+3O2↑;
(3)如果选用D收集氧气,由于氧气有助燃性,验满的方法是:将带火星的木条伸入瓶口处,若木条复燃,则证明氧气收集满了。故填:将带火星的木条伸入瓶口处,若木条复燃,则证明氧气收集满了;
(4)氧气的密度比水小,故使用装置E收集氧气时应从b管进入,故填:b;
(5)小装置B的错误是长颈漏斗末端没有形成液封,气体会沿着长颈漏斗逸出。右端导管伸入过长,气体排不出去;故填:长颈漏斗下端没有伸入液面以下,锥形瓶中导管太长。

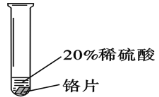
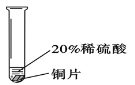
【题目】小彬同学家新买了水龙头,从说明书上了解到该水龙头是铜质镀铬的。他想起在学习金属性质时用到的金属活动性顺序中没有铬,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,进行如下探究活动。
(查阅资料) 铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜,铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液。
(猜想与假设)三种金属在金属活动性顺序中的相对位置关系:
①Cr、 Al、 Cu ② Al、 Cr、 Cu ③ Al、 Cu、 Cr
(实验过程)取大小相同的三种金属薄片,用砂纸打磨光亮。
实验一 | 实验二 | 实验三 | |
实验 方案 |
|
|
|
实验 现象 | 铬片表面产生气泡缓慢,溶液变蓝色 | _______ | 铝片表面产生气泡较快 |
结论 | 铬能和稀硫酸发生反应,反应速率较慢。 | 铜不与稀硫酸反应 | _______ |
三种金属在金属活动性由强到弱的顺序是___________ | |||
(回答问题)(1)用砂纸打磨金属片的目的是_____________。
(2)实验一所发生反应的化学方程式是____________。
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是___________。
(4)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是__________ 。
(归纳)比较金属活动性强弱的方法有①_____________ ;②______。
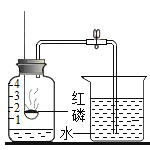
【题目】如图所示,在小烧杯A中装入30mL蒸馏水,再滴入3滴酚酞,在小烧杯B中装入30mL浓氨水,用一大烧杯把A、B两个烧杯罩在一起,过一段时间看到的现象是___________________,该实验从微观上说明___________。一些同学对上述结论有不同看法,主要有以下两种猜测:

第一种: B烧杯中的蒸馏水使酚酞试液变红
第二种: B烧杯中的浓氨水挥发出氨气,扩散到A烧杯中的溶液中生成氨水使酚酞变红。
①你认为_______________猜测正确。
②为证明这两种猜测,现设计如下实验:(请完成下空)
实验内容、方法 | 现象 | 结论 |
用洁净的烧杯取30ml水,滴入2-3滴酚酞试液,观察现象 | 不变色 | 水___________使酚酞变色(填“能”或“不能”,不同) |
取一张滤纸,滴上酚酞试液,待晾干后,放在装有浓氨水的试剂瓶上方 | 酚酞不变色 | 氨气_______________使酚酞变色 |
将少量氨气通入含有酚酞试液的蒸馏水中 | 溶液变___________色 | 氨气溶解水中形成的氨水能使酚酞变色 |
【题目】如图表示一定质量的氯酸钾和二氧化锰固体混合物受热过程中,某变量y随时间的变化趋势,纵坐标表示的是( )
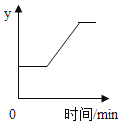
A.固体中氧元素的质量B.生成O2的质量
C.固体中MnO2的质量分数D.固体中钾元素的质量
【题目】小明同学假期在家看电视台一档“家有妙招”栏日中介绍一种“活性炭软化水”的妙招。心里泛起了嘀咕:活性炭真的可以除去硬水中钙、镁离子而使硬水软化吗?于是他到学校实验室进行了如下一系列的探究。
探究一:活性炭能否软化硬水
他按节目中介绍的方法做了一个与“妙招”制作原理相同的简易的净水装置。
(实验1)在两个体积相等的烧杯中,一个加入自来水.一个加经过简易净水器净化后的自来水,各20 ml,再分别加等体积的肥皂水,振荡,观察到的现象如下:_________。
(得出结论)用活性炭不能软化硬水。
(评价与反思)在实验中一般可通过_______来降低水的硬度,做此操作时要在烧瓶中加入几粒碎瓷片,目的是__________,日常生活中常采用煮沸方法软化水。
探究二:煮沸能否一定软化硬水
(查阅资料)
(1)水的硬度是水中所溶解的可溶性钙镁化合物引起的,硬水中所溶解的钙镁化合物可分为两类:钙、镁的碳酸氢盐,如Ca(HCO3)2等;钙、镁的硫酸盐或氯化物.如CaCl2等。一般所说水的硬度是由上述两类化合物引起的。请计算出CaCl2中钙元素化合价为_______。
(2)Ca(HCO3)2加热分解产生碳酸钙、水、二氧化碳等物质。碳酸钙难溶于水,请写出Ca(HCO3)2加热分解的反应的符号表达式____________________________
(实验2)为方便研究他准备了碳酸氢钙溶液和氯化钙溶液来代表两类不同的钙镁化合物。
实验编号 | 实验操作 | 实验现象 |
① | 分别取5ml的碳酸氢钙溶液和氯化钙溶液于A、B两支试管中,同时加热 | A试管中产生大量气泡,有沉淀产生,B试管无明显现象 |
② | 在上述实验后,分别滴加4滴肥皂水,振荡 | A试管中有大量的泡沫,B试管中泡沫较少 |
(得出结论2)煮沸实际上只能降低_______类所引起的水的硬度。
(评价与反思2)
小芳同学提出,上述实验②不做也可以得出实验的结论,理由是_________。
【题目】在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如下表:
物质 | a | b | c | d |
反应前质量(g) | 10 | 10 | 10 | 2 |
反应后质量(g) | 待测 | 2 | 21 | 2 |
(1)根据质量守恒定律,该反应中待测的质量为_______ ![]() ;
;
(2)推测该化学反应的基本类型属于_______反应,其中d可能是_______,也可能是不参与反应的其它杂质。