题目内容
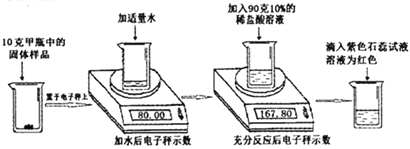
【题目】小英同学用某铁合金样品做了如下实验:称量11.4g样品,放入质量为40g的烧杯中,再往烧杯中加入200g稀硫酸,恰好完全反应(杂质不与酸反应,也不溶于水)。反应完毕后称量,烧杯及烧杯内物质总质量为251g。求:
(1)反应产生的氢气质量为__________g;
(2)所用稀硫酸的溶质质量分数________________(写出计算过程)。
【答案】 0.4 9.8%
【解析】本题考查了根据化学反应方程式的计算。根据质量守恒可知,反应过程中质量的减少是因为生成了氢气,可以求算氢气的质量,根据氢气的质量和对应的化学方程式求算硫酸的质量。
(1)由质量守恒可知,反应产生的氢气的质量是11.4g+40g+200g-251g=0.4g;
(2)设:生成0.4g的氢气需硫酸的质量为 x
Fe+H2SO4=FeSO4+H2↑
98 2
x 0.4g
![]() x=19.6g
x=19.6g
稀硫酸的溶质质量分数=![]() ×100%=9.8%。
×100%=9.8%。
答:(1)反应产生的氢气质量为0.4g;
(2)所用稀硫酸的溶质质量分数为9.8%。

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目