题目内容
32、将下列现象与相关的分子观点连线:
| 橡皮筋拉长? | ?分子保持物质的化学性质 |
| 50毫升酒精与100毫升水混合后体积<150毫升? |
?分子在不断运动、扩散 |
| 樟脑丸会不翼而飞? | ?分子间有间隙 |
| 不管是浓碘水还是稀碘水都能使淀粉变蓝? |
?分子间间隙变大 |
分析:根据分子的性质判断,分子的体积和质量都很小,在不断运动,分子间有一定的间隔,分子间隔能随温度或外力的改变而改变,同种分子性质相同,不同分子性质不同.
解答:解:橡皮筋拉长说明了分子间隔受力后变大;50毫升酒精与100毫升水混合后体积<150毫升说明分子间有间隔,酒精分子运动到水分子的间隔中;樟脑丸会不翼而飞说明分子在不断运动,樟脑分子扩散到空气中去了;不管是浓碘水还是稀碘水都能使淀粉变蓝说明同种分子性质相同,分子保持物质的化学性质.
故答案为:

故答案为:

点评:能准确利用分子的各种性质来解释日常现象,主要是分子的运动和分子的间隔用的比较多.

练习册系列答案
相关题目
某化学兴趣小组的同学设计了如下实验来验证二氧化碳气体的相关性质,实验步骤如下:
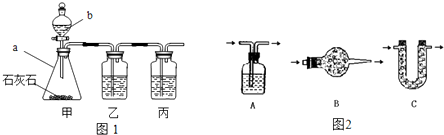
Ⅰ.取一个三通管(三个管口都未密封,与空气相通),在三通管的上部和下部各放一张湿润的蓝色石蕊试纸.然后将它与二氧化碳的发生装置连接.(如图1,整套装置的气密性良好)
Ⅱ.打开分液漏斗的活塞,使石灰石与稀盐酸接触,观察到相关现象后,停止实验.
Ⅲ.取下图1中的三通管,把贴有试纸B的那端放在酒精灯火焰上加热(如图2),观察实验现象.
注:整个实验中不考虑反应过程中水分和HCl气体的挥发,且图1中产生的气流较缓慢.
根据上述实验,回答下列问题:
(1)实验Ⅱ步骤中三通管内产生的实验现象是 ;由此说明二氧化碳气体具有 、 的性质.
(2)实验Ⅲ步骤中一定发生的化学反应方程式是 ;
(3)若不改变图1的实验装置,还要验证二氧化碳气体具有不能燃烧、也不能支持燃烧的性质,需要补充的实验是 .
(4)取12g石灰石样品放入盛有105.4g稀盐酸溶液的烧杯中,恰好完全反应.有关实验数据如下表:(假设石灰石样品中杂质不与稀盐酸反应也不溶于水,且不考虑反应过程中水分和HCl气体的挥发)
①反应中生成二氧化碳的质量为 g.
②该石灰石样品中碳酸钙的质量分数为 (结果精确到0.1%).
③反应后所得溶液中溶质质量分数是多少?(请写出计算过程)

Ⅰ.取一个三通管(三个管口都未密封,与空气相通),在三通管的上部和下部各放一张湿润的蓝色石蕊试纸.然后将它与二氧化碳的发生装置连接.(如图1,整套装置的气密性良好)
Ⅱ.打开分液漏斗的活塞,使石灰石与稀盐酸接触,观察到相关现象后,停止实验.
Ⅲ.取下图1中的三通管,把贴有试纸B的那端放在酒精灯火焰上加热(如图2),观察实验现象.
注:整个实验中不考虑反应过程中水分和HCl气体的挥发,且图1中产生的气流较缓慢.
根据上述实验,回答下列问题:
(1)实验Ⅱ步骤中三通管内产生的实验现象是
(2)实验Ⅲ步骤中一定发生的化学反应方程式是
(3)若不改变图1的实验装置,还要验证二氧化碳气体具有不能燃烧、也不能支持燃烧的性质,需要补充的实验是
(4)取12g石灰石样品放入盛有105.4g稀盐酸溶液的烧杯中,恰好完全反应.有关实验数据如下表:(假设石灰石样品中杂质不与稀盐酸反应也不溶于水,且不考虑反应过程中水分和HCl气体的挥发)
| 反应前 | 反应后 | ||
| 实验 数据 |
烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 150g | 12g | 157.6g | |
②该石灰石样品中碳酸钙的质量分数为
③反应后所得溶液中溶质质量分数是多少?(请写出计算过程)
氧化物、酸、碱、盐都是重要的无机化合物.请按要求回答下列一系列相关的问题.
(1)产生下列现象,只和空气中的水蒸气有关的是
A.固体烧碱要密封存放
B.生石灰长期在空气中放置会变质
C.浓硫酸露置于空气中会增重、变稀
D.铁制品放在潮湿空气中会生锈
(2)以下是一些食物的近似pH,对于胃酸过多的人比较适宜的食物是
(3)根据“性质决定用途,用途体现性质”回答下列问题.
A.稀释浓硫酸时,为什么不可将水倒进浓硫酸里?请简要解释其原因.
B.盐酸等许多酸都能使紫色石蕊试液变红,为什么?
C.写出用稀盐酸除水垢(主要成分是碳酸钙)的化学方程式.
(4)三支试管中分别装有少量白色固体,它们分别是氯化钠、氢氧化钠、碳酸钙中的一种,只要加入足量的 就能将它们一次性鉴别出来;盐酸(分析纯)化学式HCl质量分数36%密度l.18g/cm3
(5)实验操作考试时某同学做了如下两个实验:①氧化铜与稀硫酸反应;②烧碱溶液与酚酞溶液反应.实验结束后,该同学发现废液缸中有蓝色沉淀.请你写出有蓝色沉淀生成的反应的化学方程式是 .
(6)右图是浓盐酸试剂瓶上标签的部分内容.请回答:
A.现要配制9%的稀盐酸120g,需要这种浓盐酸 g;
B.浓盐酸使用一段时间后溶质质量分数变小的原因是什么?
C.某固体氢氧化钠在空气中敞口放置一段时间后部分变质,将该固体取10g加入质量分数为9%的盐酸至不再产生气泡为止,共产生气体质量为2.2g,试计算未变质的氢氧化钠的质量为多少克?
(1)产生下列现象,只和空气中的水蒸气有关的是
A.固体烧碱要密封存放
B.生石灰长期在空气中放置会变质
C.浓硫酸露置于空气中会增重、变稀
D.铁制品放在潮湿空气中会生锈
(2)以下是一些食物的近似pH,对于胃酸过多的人比较适宜的食物是
| 选项 | A | B | C | D |
| 物质 | 橘子 | 泡菜 | 葡萄 | 玉米粥 |
| pH | 2.9~3.5 | 3.0~4.0 | 3.5~4.5 | 6.8-8.0 |
A.稀释浓硫酸时,为什么不可将水倒进浓硫酸里?请简要解释其原因.
B.盐酸等许多酸都能使紫色石蕊试液变红,为什么?
C.写出用稀盐酸除水垢(主要成分是碳酸钙)的化学方程式.
(4)三支试管中分别装有少量白色固体,它们分别是氯化钠、氢氧化钠、碳酸钙中的一种,只要加入足量的
(5)实验操作考试时某同学做了如下两个实验:①氧化铜与稀硫酸反应;②烧碱溶液与酚酞溶液反应.实验结束后,该同学发现废液缸中有蓝色沉淀.请你写出有蓝色沉淀生成的反应的化学方程式是
(6)右图是浓盐酸试剂瓶上标签的部分内容.请回答:
A.现要配制9%的稀盐酸120g,需要这种浓盐酸
B.浓盐酸使用一段时间后溶质质量分数变小的原因是什么?
C.某固体氢氧化钠在空气中敞口放置一段时间后部分变质,将该固体取10g加入质量分数为9%的盐酸至不再产生气泡为止,共产生气体质量为2.2g,试计算未变质的氢氧化钠的质量为多少克?

 如图是某同学设计的探究空气中氧气含量的实验装置,请你协助他共同完成下列实验相关的内容.
如图是某同学设计的探究空气中氧气含量的实验装置,请你协助他共同完成下列实验相关的内容.