题目内容
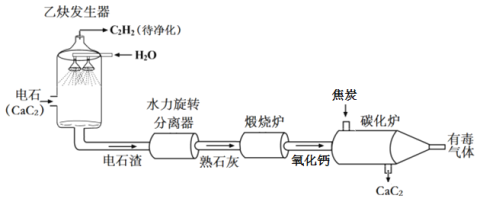
【题目】有一包固体粉末,其中含有碳酸钠、氢氧化钠、碳酸钙、生石灰、氯化钠中的四种物质。某兴趣小组为确定其组成设计并进行如下实验。
(实验一)甲组同学进行如下探究。请完成表中空白。
实验操作 | 实验现象 | 实验结论及分析 |
Ⅰ.取少量该固体粉末于烧杯中,加入足量的水溶解、过滤 | 粉末部分溶解,得到白色滤渣和无色滤液 | 滤渣中一定含有_____ |
Ⅱ.向滤液中滴加无色酚酞试液 | 溶液变红 | 滤液中可能含有_____物质(填“酸性”“碱性”或“中性”) |
Ⅲ.向Ⅱ中所得溶液滴加足量稀盐酸 | _____ | 原固体粉末中一定含有Na2CO3 |
(实验二)乙组同学进行如下探究。
取21.0g该固体粉末,加入160.0g 10%的稀盐酸,恰好完全反应,实验测得产生8.8g二氧化碳,将反应后溶液继续蒸发结晶,得到固体,测定所得固体中含16.0g氯元素。
试综合甲、乙两组同学的实验进行分析,填空:
(1)乙组实验中一定发生的化学反应是:Na2CO3+2HCl═2NaCl+H2O+CO2↑
(2)固体粉末的组成中除Na2CO3外,一定还含有的物质是_____,可能含有的物质是_____(均填写化学式)
【答案】碳酸钙 碱性 有气泡生成 CaCO3、NaCl CaO、NaOH
【解析】
实验一:由题意可知,取少量该固体粉末于烧杯中,加入足量的水溶解,由于氧化钙与水反应会生成氢氧化钙,氢氧化钙能与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,过滤,粉末部分溶解,得到白色滤渣和无色滤液,只有碳酸钙难溶于水,所以滤渣中一定含有碳酸钙;向滤液中滴加无色酚酞试液,溶液变红色,说明滤液显碱性,滤液中可能含有碱性物质;碳酸钠和盐酸反应会生成二氧化碳气体,所以,加入稀盐酸产生了大量的气泡。说明了含有碳酸钠。故填表如下:
实验操作 | 实验现象 | 实验结论及分析 |
Ⅰ.取少量该固体粉末于烧杯中,加入足量的水溶解、过滤 | 粉末部分溶解,得到白色滤渣和无色滤液 | 滤渣中一定含有碳酸钙 |
Ⅱ.向滤液中滴加无色酚酞试液 | 溶液变红 | 滤液中可能含有碱性物质 |
Ⅲ.向Ⅱ中所得溶液滴加足量稀盐酸 | 有气泡生成 | 原固体粉末中一定含有Na2CO3 |
实验二:设生成8.8g二氧化碳需要碳酸钠的质量为x,则有
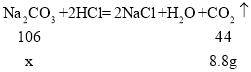
![]() 解得:x=21.2g
解得:x=21.2g
而粉末的质量只有21g,所以生成8.8g二氧化碳还需要碳酸钙,所以一定会发生碳酸钙与盐酸的反应。
160g10%的盐酸含有氯元素的质量=![]() ,而固体中含有16g氯元素,则混合物中一定含有含氯元素的物质,即一定含有氯化钠。综合以上分析可知,固体粉末的组成中除Na2CO3外,一定还含有的物质是 CaCO3、NaCl,可能含有的物质是CaO、NaOH。
,而固体中含有16g氯元素,则混合物中一定含有含氯元素的物质,即一定含有氯化钠。综合以上分析可知,固体粉末的组成中除Na2CO3外,一定还含有的物质是 CaCO3、NaCl,可能含有的物质是CaO、NaOH。

 走进文言文系列答案
走进文言文系列答案【题目】某化学学习小组在老师的指导下,对白色粉笔的成分进行探究。
(提出问题)白色粉笔的主要成分是什么呢?老师提示是一种常见的钙盐与少量性质稳定的粘合剂制成的。
(猜想与假设)同学分别做出如下猜想:
A 碳酸钙 B 氢氧化钙 C 硫酸钙 D 氯化钙 E 硝酸钙
同学们根据老师提示并讨论,立即否定了B的猜想,你认为理由是________.
(查阅资料)
(1)硫酸钙是自然界中石膏矿的主要成分,为白色固体,微溶于水.
(2)室温下几种物质的溶解度
物质 | 碳酸钙 | 氯化钙 | 硫酸钙 | 硝酸钙 |
溶解度/g | 0.0013 | 74.5 | 0.3 | 138 |
(进行实验)
实验操作 | 现象 | 结论 | |
① | 取少量白色粉笔研碎于试管中,加入________ | 无现象 | A不成立 |
② | 取少量白色粉笔研碎于烧杯中,加入少量水,搅拌 | 固体没有明显减少 | ________不成立 |
③ | 将②进行________操作,得到清液A和固体,向清液中加入 ____________溶液,再加入足量稀盐酸 | 产生白色沉淀,沉淀不消失 | C成立 |
请写出③中发生反应的化学方程式___________.
(拓展延伸)为了测定生石膏的组成(CaSO4·xH2O),即测定x的值,做了如下实验:将含结晶水的硫酸钙放在坩埚中加热,加热前和加热后都进行称量.随着实验次数的增加,加热的时间不断延长,他们在实验中将数据整理如下,并利用数据绘制的图象如图所示。
查阅资料:含结晶水的硫酸钙有两种组成形式,在加热过程中,分步失去结晶水,最终得到硫酸钙固体。
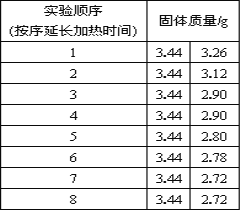

(1)AB段固体质量不变的原因__________。
(2)利用实验数据,计算x= ________.
(3)图中CD段固体物质的化学式 _____________.