题目内容
【题目】乙炔(C2H2)是有机合成的重要原料。以电石(CaC2)为原料制取乙炔,并对电石渣综合处理的生产流程如下图所示:
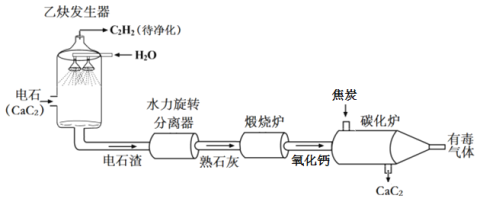
回答下列问题:
(1)分离器能除去Al2O3、Fe2O3等杂质,它们属于______(填物质类别)。
(2)煅烧炉内发生反应的基本类型为______。
(3)研究煅烧炉内氧化钙含量的变化有下图所示的结果,如果你是工作人员,你对煅烧条件的把控是_____。
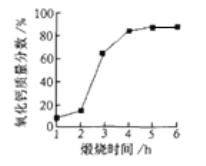
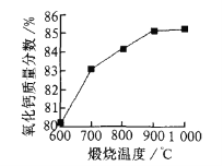
(4)乙炔发生器内发生反应的化学方程式为_____。
(5)该生产过程的尾气不能直接排放,你给尾气处理的建议是_____。
【答案】氧化物(化合物、纯净物) 分解反应 温度控制900oC,时间不少于4-5小时 CaC2+2H2O===Ca(OH)2+C2H2↑ 回收做燃料
【解析】
(1)氧化铝、氧化铁都含有两种元素且有一种元素是氧元素,属于氧化物;
(2)氢氧化钙和二氧化碳反应生成碳酸钙,煅烧炉发生的是碳酸钙高温分解生成氧化钙和二氧化碳的反应,该反应符合“一变多”的特征,属于分解反应;
(3)根据图表信息可知,煅烧时间达到4-5小时氧化钙质量分数接近并达到最大值,煅烧温度大于900℃时氧化钙质量分数达到最大值,所以温度控制900oC,时间不少于4-5小时;
(4)乙炔发生器内发生的是碳化钙和水反应生成氢氧化钙和乙炔,反应的化学方程式为CaC2+2H2O===Ca(OH)2+C2H2↑;
(5)该生产过程的尾气含有有毒的一氧化碳,不能直接排放,由于一氧化碳具有可燃性,可以回收做燃料。

 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案【题目】有一包固体粉末,其中含有碳酸钠、氢氧化钠、碳酸钙、生石灰、氯化钠中的四种物质。某兴趣小组为确定其组成设计并进行如下实验。
(实验一)甲组同学进行如下探究。请完成表中空白。
实验操作 | 实验现象 | 实验结论及分析 |
Ⅰ.取少量该固体粉末于烧杯中,加入足量的水溶解、过滤 | 粉末部分溶解,得到白色滤渣和无色滤液 | 滤渣中一定含有_____ |
Ⅱ.向滤液中滴加无色酚酞试液 | 溶液变红 | 滤液中可能含有_____物质(填“酸性”“碱性”或“中性”) |
Ⅲ.向Ⅱ中所得溶液滴加足量稀盐酸 | _____ | 原固体粉末中一定含有Na2CO3 |
(实验二)乙组同学进行如下探究。
取21.0g该固体粉末,加入160.0g 10%的稀盐酸,恰好完全反应,实验测得产生8.8g二氧化碳,将反应后溶液继续蒸发结晶,得到固体,测定所得固体中含16.0g氯元素。
试综合甲、乙两组同学的实验进行分析,填空:
(1)乙组实验中一定发生的化学反应是:Na2CO3+2HCl═2NaCl+H2O+CO2↑
(2)固体粉末的组成中除Na2CO3外,一定还含有的物质是_____,可能含有的物质是_____(均填写化学式)
【题目】小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度。于是他对所得溶液的酸碱性进行探究。
(实验探究)稀盐酸与氢氧化钠反应的化学方程式为_____。
(提出猜想)所得溶液可能呈碱性,也可能呈_____性,还可能呈_____性。
(实验验证)
实验操作 | 实验现象 | 结论 |
用试管取该溶液1﹣2mL,滴入 1﹣2滴无色酚酞试液,振荡 | 无色酚酞试液变_____ | 溶液呈碱性 |
无色酚酞试液不变色 | 溶液呈_____ |
若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
取样,加入金属锌,若有所泡产生,则所取溶液呈酸性,该反应的化学方程式为_____;若无明显现象,则溶液呈_____性。
(分析论证)如图是小亮同学根据实验绘制的溶液的pH随加入溶液的质量变化的曲线。
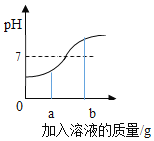
①氢氧化钠与盐酸恰好完完全反应时,溶液的pH_____7(填“>“<”或“=”)
②根据曲线判断,小亮是将_____(填“氢氧化钠溶液”或“盐酸”,下同)滴入_____中。
③当滴入溶液的质量为bg时,向所得溶液中滴加酚酞溶液,溶液颜色为_____色,此时溶液中的溶质是_____、_____。