题目内容
【题目】宏观和微观相结合是认识物质结构的有效方法之一。
已知:X、Y、Z、W四种粒子的核电荷数及核外各电子层电子排布情况如下表。
X | Y | Z | W | U | ||
对应元素名称 | 氧 | 镁 | 铝 | 氯 | 氩 | |
核电荷数 | 8 | 12 | 13 | 17 | 18 | |
电子层 | 第一层 | 2 | 2 | 2 | 2 | 2 |
第二层 | 6 | 8 | 8 | 8 | 8 | |
第三层 | a | 8 | 8 | |||
请回答下列问题
(1)若Z表示原子,a=_______。 单质X2与单质Z的反应中,Z原子______(填“得到”或“失去”电子。
(2)具有相对稳定结构的原子是_______(填粒子符号)
(3)Y、W形成的化合物溶解于水形成的水溶液易导电,因为该化合物溶解于水会解离出_____________(用离子符号表示)。
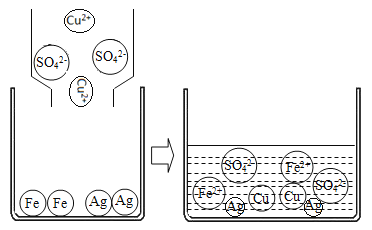
(4)将硫酸铜溶液与烧杯中Fe、Ag两种金属相混合,微观变化情况如图:则变化过程中的微观反应实质是___________,并写出本质相同的另一个化学反应方程式_____________(反应物之一必须为铁)。
【答案】3 失去 Ar Mg2+ 、Cl- Fe+Cu2+=Cu+Fe2+ Fe+2AgNO3=2Ag+Fe(NO3)2
【解析】
(1)原子中电子数=核电荷数;原子最外层电子数小于4个,容易失去电子。
(2)最外层电子数为8是相对稳定结构。
(3)Y、W形成的化合物是氯化镁,溶解于水形成的水溶液易导电,因为该化合物溶解于水会解离出镁离子和氯离子。
(4)铁和硫酸铜反应生成铜和硫酸亚铁,微观反应实质是Fe+Cu2+=Cu+Fe2+。
(1) Z表示铝原子,根据电子数=核电荷数,a=13-2-8=3。 单质X2与单质Z的反应中,Z原子最外层电子数小于4个,容易失去3个电子。
(2)最外层电子数为8是相对稳定结构,具有相对稳定结构的原子是氩原子Ar。
(3)Y、W形成的化合物是氯化镁,溶解于水形成的水溶液易导电,因为该化合物溶解于水会解离出镁离子和氯离子,即Mg2+ 、Cl-。
(4)将硫酸铜溶液与烧杯中Fe、Ag两种金属相混合,微观变化情况如图:则变化过程中的微观反应实质是Fe+Cu2+=Cu+Fe2+,并写出本质相同的另一个化学反应方程式即铁和盐溶液反应,如Fe+2AgNO3=2Ag+Fe(NO3)2。

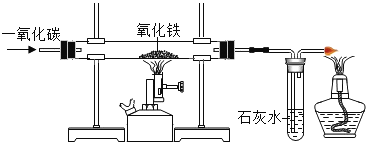
【题目】如图A为碳还原氧化铜的实验装置图。老师指出反应物不同的质量比可能会影响生成物的种类,在学习时,可以从定性观察和定量分析两个角度来判断生成物。请你跟随老师的思路,探究碳还原氧化铜生成的气体.(浓硫酸具有吸水性)
(提出问题):碳还原氧化铜生成的气体是什么?
(作出猜想):猜想①:CO 猜想②:CO2 猜想③:_____
(实验设计):装置图如图:
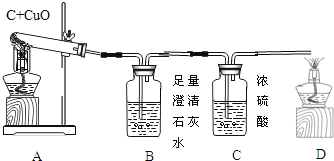
方案一:从定性观察角度判断:
若猜想3成立B处的现象是_____,D处发生反应的化学反应方程式_____
方案二:从定量计算角度判断:
测定表格中的四个数据:
反应前的质量 | 反应后的质量 | |
装置A | m1 | m2 |
装置B | m3 | m4 |
Ⅰ、若猜想②成立,则m4m3_____m1m2(选填“>”、“<”或“=”),此时A中的现象是_____;B发生反应的化学方程式为_____
Ⅱ、实际测量中B增加的质量小于理论值,请你分析可能的原因_____