题目内容
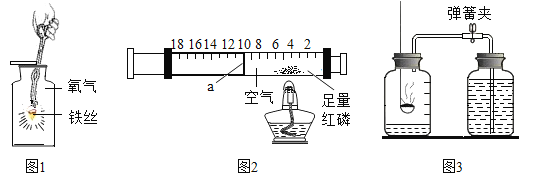
【题目】下图是实验室制取气体的部分装置。
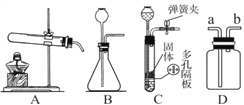
(1)写出一个用A装置制取气体的化学方程式_______。
(2)B和C装置均可制取气体,其中C装置的优点是什么?_______
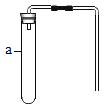
(3)若用排水法收集氢气,可以先在D集气瓶中装满水,再从________(选填“a”或“b”)导管通入氢气。
【答案】 2KMnO4 ![]() K2 MnO4 + MnO2 + O2 ↑ ( 或2KClO3
K2 MnO4 + MnO2 + O2 ↑ ( 或2KClO3![]() 2KCl + 3O2 ↑) 可随时控制反应的发生与停止 b
2KCl + 3O2 ↑) 可随时控制反应的发生与停止 b
【解析】(1).选择发生装置需考虑是因素是,反应物的状态和反应条件。加热固体制取气体,发生装置为A,高锰酸钾法或氯酸钾法制取氧气可以用A装置;反应方程式为:2KMnO4 ![]() K2 MnO4 + MnO2 + O2 ↑ ( 或2KClO3
K2 MnO4 + MnO2 + O2 ↑ ( 或2KClO3 ![]() 2KCl + 3O2 ↑) (2)B和C装置均可制取气体,其中C装置的优点是:可随时控制反应的发生与停止。原理是关闭弹簧夹,大试管内气体增多,压强变大,在压力的作用下,试管内液面下降,当液面下降到隔板下边时,固体反应物与液体分离,反应停止;反之,打开弹簧夹,反应开始。(3)氢气的密度比水的小,若用排水法收集氢气,可以先在D集气瓶中装满水,再从b导管通入氢气。
2KCl + 3O2 ↑) (2)B和C装置均可制取气体,其中C装置的优点是:可随时控制反应的发生与停止。原理是关闭弹簧夹,大试管内气体增多,压强变大,在压力的作用下,试管内液面下降,当液面下降到隔板下边时,固体反应物与液体分离,反应停止;反之,打开弹簧夹,反应开始。(3)氢气的密度比水的小,若用排水法收集氢气,可以先在D集气瓶中装满水,再从b导管通入氢气。
点睛:将实验装置和制取气体的情况对照,选择合适发生装置和收集装置。
【题型】实验题
【结束】
24
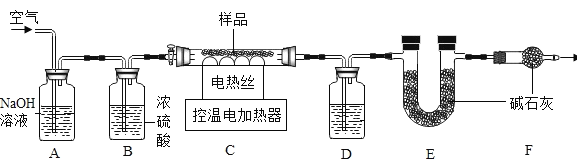
【题目】实验室模拟工业炼铁的装置图如图所示。
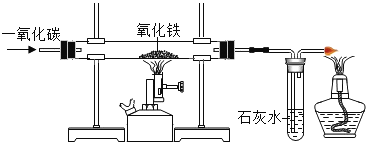
(1)写出一氧化碳与氧化铁反应的化学方程式__________________。
(2)写出硬质玻璃管中的现象__________________。
(3)写出最右侧酒精灯的作用__________________。
【答案】Fe2O3+3CO![]() 2Fe+3CO2 红色粉末逐渐变黑 点燃尾气,防止CO污染空气
2Fe+3CO2 红色粉末逐渐变黑 点燃尾气,防止CO污染空气
【解析】
(1)由题意可知,在高温条件下,一氧化碳能与氧化铁反应,生成了铁和二氧化碳。反应的方程式是:Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
(2)由于氧化铁是红色的,生成的铁粉是黑色的。所以,硬质玻璃管中的现象是:红色粉末逐渐变黑;
(3)由于尾气中含有的一氧化碳有毒能污染空气。所以,最右侧酒精灯的作用是:点燃尾气,防止CO污染空气。
故答案为:Fe2O3+3CO![]() 2Fe+3CO2;红色粉末逐渐变黑;点燃尾气,防止CO污染空气。
2Fe+3CO2;红色粉末逐渐变黑;点燃尾气,防止CO污染空气。

【题目】(1)小明在帮老师整理实验室时,发现一瓶未密封的NaOH固体,对其成分提出以下假设,并在老师的指导下进行实验探究
(查阅资料):①NaOH暴露在空气中易变质请用化学方程式解释NaOH变质的原因_____
②Na2CO3溶液呈碱性,BaCl2溶液NaCl溶液呈中性
(猜想假设):假设I:只含NaOH;假设Ⅱ:含NaOH和Na2CO3;假设Ⅲ:只含Na2CO3
(进行实验):
实验操作步骤 | 实验现象 | 实验结论 |
①取少量样品于试管中,加入足量的稀盐酸 | 有气泡产生 | 假设_____不正确 |
②另取少量样品于试管中,加水溶解,加入 过量的BaCl2溶液,振荡,静置 | _____ | 假设Ⅲ正确 |
③取②中上层清液,滴加无色酚酞溶液 | _____ |
(问题讨论):步骤②中加入过量BaCl2溶液的作用是_____,如将②中BaCl2溶液换成Ba(OH)2溶液,实验能否成功?_____(填“能”或“不能”),原因是_____
(2)小红为了测定一瓶未密封保存已部分变质的NaOH固体中NaOH的质量分数,采用沉淀法进行如下操作:①取15克样品于烧杯中,加足量水配成溶液;
②在样品溶液中加入足量的BaCl2溶液;
③待反应完全后,过滤有关数据记录如下表:
反应前 | 反应后 | |
烧杯和样品溶液总质量/g | 加入氯化钡溶液质量/g | 过滤后烧杯和溶液总质量/g(滤液的损失忽略不计) |
95 | 65 | 140.3 |
请回答下列问题:
①在反应前后的溶液中,下列元素质量保持不变的是_____
A钠元素 B碳元素 C钡元素 D氧元素
②原样品中NaOH的质量分数是多少?(写出计算过程)_____
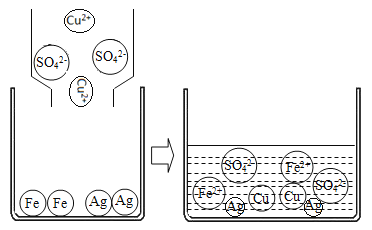
【题目】宏观和微观相结合是认识物质结构的有效方法之一。
已知:X、Y、Z、W四种粒子的核电荷数及核外各电子层电子排布情况如下表。
X | Y | Z | W | U | ||
对应元素名称 | 氧 | 镁 | 铝 | 氯 | 氩 | |
核电荷数 | 8 | 12 | 13 | 17 | 18 | |
电子层 | 第一层 | 2 | 2 | 2 | 2 | 2 |
第二层 | 6 | 8 | 8 | 8 | 8 | |
第三层 | a | 8 | 8 | |||
请回答下列问题
(1)若Z表示原子,a=_______。 单质X2与单质Z的反应中,Z原子______(填“得到”或“失去”电子。
(2)具有相对稳定结构的原子是_______(填粒子符号)
(3)Y、W形成的化合物溶解于水形成的水溶液易导电,因为该化合物溶解于水会解离出_____________(用离子符号表示)。
(4)将硫酸铜溶液与烧杯中Fe、Ag两种金属相混合,微观变化情况如图:则变化过程中的微观反应实质是___________,并写出本质相同的另一个化学反应方程式_____________(反应物之一必须为铁)。