题目内容
【题目】下图是初中化学常见物质的转化关系,其中B常用于改良酸性土壤,J是常见金属,G是红色物质,D的溶液能与硝酸银溶液反应产生不溶于稀硝酸的白色沉淀。请回答下列问题:
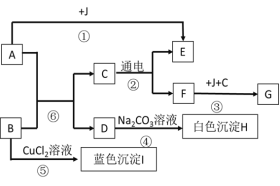
(1)F、I的化学式分别为:_____、____
(2)B物质的俗名是:_____。
(3)H的用途是______,反应⑤的基本反应类型是_____。
(4)写出①⑥反应的化学方程式:①__________;⑥_________。
【答案】O2 Cu(OH)2 熟石灰 作建筑材料 复分解反应 Fe+2HCl═FeCl2+H2↑ Ca(OH)2+2HCl═CaCl2+2H2O
【解析】
根据B用于改良酸性土壤,说明B是氢氧化钙,其化学式为Ca(OH)2;根据图框,C通电能生成E和F两种无色气体,说明C是水,E和F是氢气和氧气;在溶液D中滴入AgNO3溶液产生难溶于硝酸的白色沉淀,说明D中含有氯离子,则A可能是盐酸,D是氯化钙,所以白色沉淀H为碳酸钙,其化学式为CaCO3;J是常见的金属,可以知道J为铁,J与水和氧气能生成红棕色物质G,则F为氧气,可以判断G为氧化铁;代入检验。
(1)根据分析,F、I的化学式分别为:O2、Cu(OH)2。
(2)根据分析,B物质俗称熟石灰;
(3)根据分析,H为碳酸钙,H的用途作建筑材料,反应⑤的基本反应类型氢氧化钙与氯化铜溶液反应生成氯化钙和氢氧化铜沉淀,该反应为复分解反应;
(4)反应①为铁与稀盐酸反应生成氯化亚铁和氢气,反应的化学方程式为:Fe+2HCl═FeCl2+H2↑;
反应⑥为氢氧化钙与稀盐酸反应生成氯化钙和水,反应的化学方程式为:Ca(OH)2+2HCl═CaCl2+2H2O。
故答案为:
(1)O2、Cu(OH)2.(2)熟石灰。(3)作建筑材料,复分解反应。(4)①Fe+2HCl═FeCl2+H2↑;⑥Ca(OH)2+2HCl═CaCl2+2H2O。

 特高级教师点拨系列答案
特高级教师点拨系列答案【题目】为测定某地石灰石中碳酸钙的质量分数,某兴趣小组将一定质量的石灰石样品粉碎后分成两等份,进行如下实验:
(1)一份放于烧杯中,向烧杯中逐渐加入某一浓度的盐酸,反应过程测得剩余固体质量与加入盐酸的质量关系如图所示(石灰石中的杂质不与盐酸反应,也不溶与水)。请回答下列问题:
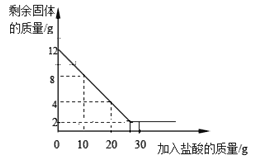
①石灰石样品中碳酸钙的质量分数________;
②通过计算求所用盐酸的溶质质量分数为__________。
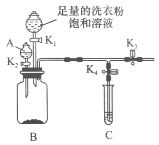
(2)另一份进行如下图所示的实验:把产生的CO2气体用足量的烧碱溶液吸收,同时测量B瓶烧碱溶液增加的质量,结果如下表所示:
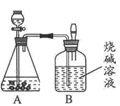
时间/分 | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
B增加的质量 | 0 | 2 | 3 | 4 | 4.6 | X | 4.6 |
①右上表中,第5分钟时,x=______________;
②该实验测得样品中碳酸钙的质量分数_________(填大于、小于或等于)另一实验,其原因可能是______________________________。