题目内容
【题目】实验室有一瓶久置的氧化钙,经测定该固体中氢元素的质量分数为0.8%,碳元素的质量分数为2.4%。则已变质的氧化钙占变质前纯氧化钙的质量分数为
A.80%B.66.7%C.40%D.18.8%
【答案】C
【解析】
设久置的氧化钙固体的质量为100g,含有碳元素的质量为100g×2.4%=2.4g,则含有的碳酸钙的质量为:2.4g÷![]() =20g;
=20g;
设生成碳酸钙所消耗的氢氧化钙的质量为x,则有
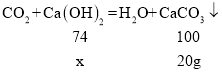
![]()
x=14.8g
则含有氢元素的质量为100g×0.8%=0.8g,则久置固体中的氢氧化钙的质量为:0.8g÷![]() =29.6g;
=29.6g;
设共变质的氧化钙的质量为y,则有
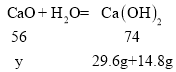
![]()
![]()
y=33.6g
因此原固体中氧化钙的总质量=久置固体质量-碳酸钙的质量-氢氧化钙的质量+变质的氧化钙的质量=100g-20g-29.6g+33.6g=84g,已变质的氧化钙占变质前纯氧化钙的质量分数为:
![]() 。
。
故选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目