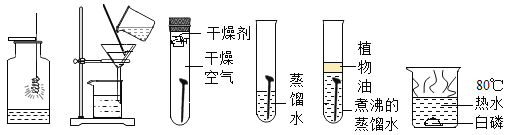
题目内容
【题目】金属是人类利用最广泛的材料之一,请用所学的化学知识回答下列问题。
(1)生铁和钢都是铁的合金,其区别是_____。
(2)铝在常温下易与空气中的氧气反应生成一层致密的保护膜,因而铝具有良好的抗腐蚀性能,该保护膜的成分是_____。
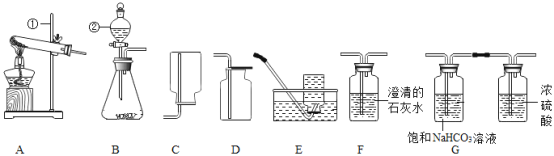
(3)如图为某学习小组探究金属化学性质时所做的四个实验,仔细分析后回答下列问题:
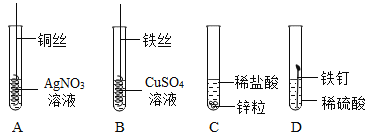
①描述A中的实验现象_____。
②写出C中反应的化学方程式_____。
③要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是_____(填序号)。
④开始反应后D中溶液逐渐变为黄色,原因是_____(化学方程式)。
(4)某课外小组采集到一批铁矿石标本,经检测后发现该矿石中Fe2O3的质量分数为80%,若用300t该矿石,理论上可冶炼出铁含量为96%的生铁的质量是_____。
(5)在Fe(NO3)2和AgNO3的混合溶液中,加入一定量的锌粉,充分反应后过滤,,得到滤渣和滤液。下列说法中正确的是_____(填序号)。
a、若滤液为浅绿色,则滤渣中可能有锌
b、滤液中一定有Zn(NO3)2,滤渣中一定有银
c、若取少量滤液,加入KC1溶液,无明显现象,则滤渣中一定有铁
d、若取少量滤渣,加入稀盐酸,产生气泡,则滤渣的组成有三种情况
(6)将10g氧化铜和铜的混合物放入烧杯中,加入100g溶质质量分数为7.3%的稀盐酸,恰好完全反应,则原10g氧化铜和铜的混合物中铜元素的质量分数为_____。
【答案】含碳量不同 A12O3 铜丝表面有银白色固体析出,溶液由无色变蓝色 ![]() AB
AB ![]() 175t b 84%
175t b 84%
【解析】
(1)生铁的含碳量在2%~4.3%之间,钢的含碳量在0.03%~2%之间,即生铁与钢的区别是含碳量不同,故填含碳量不同。
(2)铝的化学性质比较活泼,在常温下就能与空气中的氧气反应生成致密的氧化铝,对内层的铝起保护作用,氧化铝的化学式为A12O3,故填A12O3。
(3)①A中的反应是铜与硝酸银反应生成银和硝酸铜,观察到的现象是铜丝表面有银白色固体析出,溶液由无色变蓝色,故填铜丝表面有银白色固体析出,溶液由无色变蓝色;
②C中的反应是锌与稀盐酸反应生成氯化锌和氢气,故反应的化学方程式写为:Zn+2HCl=ZnCl2+H2↑;
③A实验中铜能够与硝酸银反应生成银和硝酸铜,证明铜的活动性比银强,B实验中铁能够与硫酸铜反应生成硫酸亚铁和铜,证明铁的活动性比铜强,要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是AB,故填AB;
④开始反应后D中溶液逐渐变为黄色是因为铁钉表面的铁锈中的氧化铁与硫酸反应生成硫酸铁和水,硫酸铁溶于水后溶液呈黄色,故反应的化学方程式写为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O。
(4)设可冶炼出铁含量为96%的生铁的质量为x
300t×80%×![]() ×100%=x×96%
×100%=x×96%
x=175t,故填175t。
(5)a 若滤液为浅绿色,滤液中一定含有硝酸亚铁,则反应中锌的量不足,没有将硝酸亚铁完全置换,则滤渣中一定没有锌,选项错误;
b 加入的锌粉先与活动性较弱的银的盐溶液硝酸银反应生成银和硝酸锌,所以滤液中一定有Zn(NO3)2,滤渣中一定有银,选项正确;
c 若取少量滤液,加入KC1溶液,无明显现象,证明硝酸银完全与锌反应生成了银和硝酸锌,则滤渣中一定有银,不能判断是否含有铁,选项错误;
d 题目中出现的金属中只有锌、铁能够与稀盐酸反应产生气泡,若取少量滤渣,加入稀盐酸,产生气泡,则滤渣可能的组成有银、铁或银、铁、锌两种情况,选项错误,故填b。
(6)参加反应的纯净HCl的质量=100g×7.3%=7.3g
设样品中氧化铜的质量为x
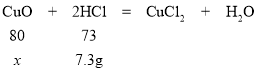
80:73=x:7.3g x=8g
氧化铜中铜元素的质量=8g×![]() ×100%=6.4g
×100%=6.4g
原10g氧化铜和铜的混合物中铜元素的质量分数=![]() ×100%=84%
×100%=84%
答:原10g氧化铜和铜的混合物中铜元素的质量分数为84%。

 高效智能课时作业系列答案
高效智能课时作业系列答案【题目】下列表中各物质不能按照图中关系(“→”表示反应一步完成)转化的是
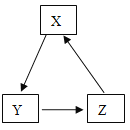
物质选项 | A | B | C | D |
X | Na2SO4 | BaCl2 | Cu | CaO |
Y | NaCl | Ba(NO3)2 | CuO | CaCl2 |
Z | NaNO3 | BaCO3 | CuSO4 | CaCO3 |
A.AB.BC.CD.D