题目内容
【题目】小明同学在某化工厂进行社会实践,技术员与小明一起分析由氯化钙和氯化钠组成的产品中氯化钠的含量。现取13.4g固体样品,全部溶于96.6g水中,向所得的混合溶液中滴加溶质质量分数为10.6%的碳酸钠溶液,记录了如图所示的曲线关系。技术员提示小明:氯化钙与碳酸钠反应的化学方程式:CaCl2+Na2CO3 =CaCO3↓+2NaCl。求:
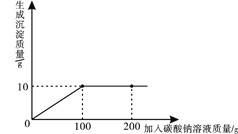
(1)样品中氯化钠的质量是多少?
(2)当氯化钙与碳酸钠恰好完全反应时,过滤,所得溶液中溶质的质量分数是多少?
【答案】2.3g。
@7%
【解析】(1)混合溶液中的氯化钙能与碳酸钠溶液反应生成碳酸钙沉淀,氯化钠不与碳酸钠反应。设样品中氯化钙的质量是x。
CaCl2+Na2CO3 =CaCO3↓+2NaCl
111 100
x 10g
![]() =
=![]() ,解答x=11.1g
,解答x=11.1g
所以样品中氯化钠的质量是:13.4g-11.1g=2.3g
(2)设氯化钙与碳酸钠恰好完全反应时生成氯化钠的质量为y。
CaCl2+Na2CO3 =CaCO3↓+2NaCl
100 117
10g y
![]() =
=![]() ,解答y=11.7g
,解答y=11.7g
滤液中氯化钠的质量为:11.7g+2.3g=14g
当氯化钙与碳酸钠恰好完全反应时,过滤,所得滤液的质量是:13.4g+96.6g+100g-10g=200g
所以恰好反应时所得滤液中溶质的质量分数是:![]() ×100%=7%
×100%=7%

【题目】下列关于反应类型和物质类别的判断不完全正确的是( )
选项 | 化学方程式 | 反应类型 | 所选物质类别 |
A | FeCl3+3NH3H2O=Fe(OH)3↓+3NH4Cl | 复分解反应 | NH3H2O是碱 |
B | 3C+2Fe2O3 | 置换反应 | Fe是金属单质 |
C | 4NO2+O2+2H2O═4HNO3 | 化合反应 | HNO3是酸 |
D | 2KClO3 | 分解反应 | KClO3是氧化物 |
A. A B. B C. C D. D
【题目】下列有关化学反应类型的判断,错误的是
选项 | 化学方程式 | 反应类型 |
A | 4Fe(OH)2+O2+2H2O = 4Fe(OH)3 | 化合反应 |
B | 2NaHCO3 | 分解反应 |
C | BaCl2+2AgNO3=2AgCl↓+Ba(NO3)2 | 复分解反应 |
D | Fe3O4+4CO | 置换反应 |
A. A B. B C. C D. D