题目内容
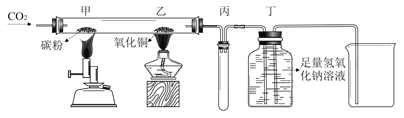
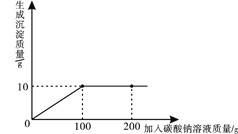
【题目】硅钢合金是变压器、充电器中的核心材料,其主要成份是铁和硅。向8.4g硅钢中加入100g稀硫酸,恰好完全反应(硅及其杂质不溶于水,且都不与稀硫酸反应),放出气体的质量与反应时的关系如图所示。

试回答:(计算结果精确到0.1% )
(1)硅钢合金属于____________材料(选填“金属”或“有机物”)
(2)硅钢合金中铁的质量分数为_________。
(3)反应结束后所得溶液溶质质量分数为_________。
【答案】 金属 83.3% 17.9%
【解析】本题主要考查了化学方程式和质量分数相结合的计算。读懂图像的涵义是解题的关键。
(1)硅钢合金属于金属材料;
解:(2)设8.4g硅钢中铁的质量为x,生成硫酸亚铁的质量为y,
根据图像可知反应生了0.25g的氢气。
Fe+H2SO4═FeSO4+H2↑
56 152 2
x y 0.25g
![]()
![]()
x=7g,y=19g,
硅钢合金中铁的质量分数为: ![]() ×100%=83.3%,
×100%=83.3%,
答:硅钢合金中铁的质量分数为83.3%。
(3)反应结束后所得溶液溶质质量分数=![]() ×100%=17.8%,
×100%=17.8%,
答:反应结束后所得溶液溶质质量分数是17.8%。

【题目】下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g 水)。
温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
①20℃时溶解度较大的物质是_________ ;
②除去KNO3晶体中混有的少量 NaCl,通过溶解、蒸发浓缩、______、过滤、洗涤、干燥得到比较纯净的KNO3晶体。滤液中溶质的成分有___________。
③用 4 只小烧杯取 T℃时的水各 50 克,进行实验并记录数据如下:
实验编号 | 1 | 2 | 3 | 4 |
KNO3 质量/g | 40 | 50 | 60 | 70 |
H2O质量/g | 50 | 50 | 50 | 50 |
溶液质量/g | 90 | 100 | 105 | X |
Ⅰ.实验 1 所得溶液的质量分数为_______ ,实验 4 中 X 的值为 _________,
Ⅱ. T℃时KNO3 的溶解度是 _________ g/100g 水。