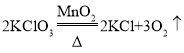题目内容
【题目】如图是以化合价为纵坐标,物质的类别为横坐标绘制的价类图。图中A-M是初中化学常见的九种物质(图中“→”表示一种物质转换成另一种物质),已知A和水反应放出大量的热,F中含有二种元素。
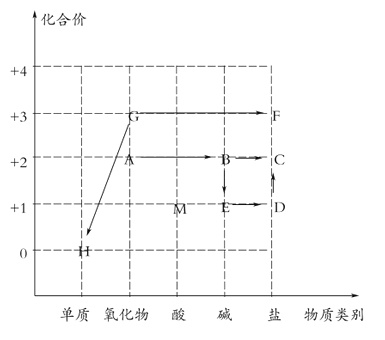
请回答下列问题:
(1)H的名称是______________。
(2)H、G均可与M溶液反应,分别生成含该金属元素的两种盐溶液。M与A反应的化学方程式为______________。
(3)D是由四种元素组成的化合物,向D溶液中加入一定量的B溶液,产生白色沉淀。过滤后取滤液,滴入过量M溶液,无明显现象,则滤液中的溶质是______________。(写出所有可能情况,填化学式)
(4)A-H八种物质中不能与M溶液反应的物质是______________。(填化学式)
(5)D→C反应的化学方程式为______________。
【答案】铁 ![]() NaOH或NaOH和Ca(OH)2 FeCl3
NaOH或NaOH和Ca(OH)2 FeCl3 ![]()
【解析】
A是能和水反应放出大量的热的氧化物,所以A是氧化钙,转化生成的B属于碱,是氢氧化钙,氢氧化钙转化生成的C是碳酸钙;氢氧化钙转化生成的E能转化生成D,最终转化生成碳酸钙,且D是由四种元素组成的化合物所以E是氢氧化钠,D是碳酸氢钠;H是单质,能与M反应,G是H的+3氧化物,分别与酸反应生成含该金属元素的两种盐溶液,则H是铁,G是氧化铁,G生成的含有两种元素的盐F是氯化铁,M是常用的酸,盐酸。代入验证符合。
(1)根据分析知,H的名称是铁。
(2)H、G均可与M溶液反应,分别生成含该金属元素的两种盐溶液,M是盐酸,M与A氧化钙反应的化学方程式为![]() 。
。
(3)D是由四种元素组成的化合物,结合分析知D是碳酸氢钠,向D溶液中加入一定量的B氢氧化钙溶液,产生白色沉淀碳酸钙和氢氧化钠。过滤后取滤液,滴入过量M盐酸溶液,无明显现象,说明碳酸氢钠反应完全,氢氧化钙可能恰好反应完,也有可能有剩余,则滤液中的溶质是NaOH或NaOH和Ca(OH)2。
(4)M是酸,酸可以与活泼金属发生置换反应,与金属氧化物反应,也可以与碱发生中和反应,D是碳酸氢钠,C是碳酸钙,二者都能与酸反应生成二氧化碳,A-H八种物质中不能与M溶液反应的物质是F氯化铁,化学式为:FeCl3。
(5)D→C反应的化学方程式为![]() 。
。

 灵星计算小达人系列答案
灵星计算小达人系列答案【题目】小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度。于是他对所得溶液的酸碱性进行探究。
[探究目的]探究所得溶液的酸碱性
[提出猜想]所得溶液可能呈碱性,也可能呈中性,还可能呈酸性。
[实验验证]
实验操作 | 实验现象 | 结论 |
用试管取该溶液1 -2 mL,滴入1~2滴无色酚酞试液,振荡 | 无色酚酞试液变____ | 溶液呈碱性 |
无色酚酞试液不变色 | 溶液呈____ |
[分析与思考]
(1)若溶液呈碱性,则溶液中使其呈碱性的离子是____ ( 填写微粒符号) ,为避免碱性溶液污染环境,小亮对所得溶液进行了如下处理:向溶液中逐滴加入_____溶液,直到不再产生沉淀为止。然后过滤。把滤液倒入蒸发皿中加热,得到氯化钠晶体,该过程涉及的化学方程式为___
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入碳酸钠溶液,若观察到_____,则所取溶液呈酸性;若无明显现象,则呈中性。
方案二:取样,加入金属锌,若有气泡产生,则所取溶液呈酸性,该反应的化学方程式为__;若无明显现象,则呈中性。