题目内容
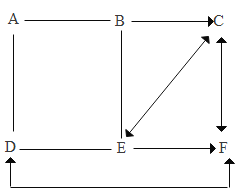
【题目】如图所示A~F是初中化学常见的物质。图中“→”表示转化关系,“一”表示相互能反应,( 部分物质和反应条件未标出)。其中A、D、E分别属于酸、碱、盐中的某一种,B、 C属于单质且B是应用最广泛的金属,E是人体胃液的主要成分。
请回答下列问题:
(1)写出下列物质的化学式;C_________,D_______, E_______,F________。
(2)F→D反应的化学方程式为_____________________。
(3)B与E反应的实验现象为_______________。
【答案】H2 Ca(OH)2 HCl H2O CaO + H2O = Ca(OH)2 银白色固体减少,有气泡产生,放热,溶液颜色由无色变为浅绿色
【解析】
B是应用最广泛的金属,则B为铁,E是人体胃液的主要成分,则E为盐酸,A、D、E分别属于酸、碱、盐中的某一种,A、D属于酸或碱,A能与B(铁)反应,则A为盐,铁能与硫酸铜反应,可能是硫酸铜,D为碱,可能是氢氧化钠或氢氧化钙;E能转化为F,F能转化为D(可能氢氧化钠或氢氧化钙),氧化钙与水反应能生成氢氧化钙,盐酸与氢氧化钙反应生成氯化钙和水,所以D是氢氧化钙,F是水;F(水)与C能相互转化,B(铁)能转化为C,水通电分解生成氢气和氧气,氢气在氧气中燃烧生成水,铁与盐酸反应生成氯化亚铁和氢气,所以C为氢气,代入关系图,猜想成立。
根据以上分析可知:
(1)C是氢气,化学式为:H2,D是氢氧化钙,化学式为:Ca(OH)2;, E是盐酸,化学式为:HCl,F是水,化学式为:H2O。
(2)F→D的反应是氧化钙与水反应生成氢氧化钙,反应的化学方程式为:CaO + H2O = Ca(OH)2;
(3)B与E的反应是铁与盐酸反应生成氯化亚铁和氢气,实验现象为银白色固体减少,有气泡产生,放热,溶液颜色由无色变为浅绿色。

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案【题目】某水泥厂新进一批石灰石原料,该厂检验室为了测定该石灰石中碳酸钙的质量分数,取该样品 12g 与足量稀盐酸在烧杯中恰好完全反应(假设石灰石样品中的杂质不与稀盐酸反应,而且也不溶于水),有关实验数据如表:(烧杯的质量为 82g)
反应前 | 反应后 | ||
实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的总质量 |
152.0g | 12.0g | 159.6g | |
(1)反应中生成二氧化碳的质量为_____;
(2)求该石灰石中碳酸钙的质量分数;(结果保留一位小数) _________
(3)反应后所得溶液的溶质的质量分数是多少?(结果保留一位小数) _________