题目内容
【题目】下图是甲、乙、丙三种固体物质的溶解度曲线,下列说法不正确的是
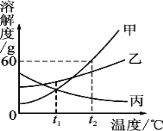
A. t2℃100 g甲物质饱和溶液中含有60 g甲
B. t2℃时,三种固体物质的溶解度关系为甲>乙>丙
C. 将丙物质不饱和溶液变为饱和溶液,可采用升温的方法
D. t2℃时,分别用100 g水配制甲、乙的饱和溶液,再降温到t1℃,析出固体的质量:甲>乙
【答案】A
【解析】
A、由图可知,t2℃时甲物质的溶解度为60g,则此时含有60 g甲物质的饱和溶液的质量应为160g,选项错误;
B、由图可知,t2℃时,三种固体物质的溶解度曲线由高到低的顺序是甲、乙、丙,所以三种物质的溶解度关系为甲>乙>丙,选项正确;
C、由图可知,丙物质的溶解度随温度升高反而减小,所以将丙物质不饱和溶液变为饱和溶液,可采用升温的方法,选项正确;
D、由图可知,甲物质的溶解度受温度影响比乙物质受温度影响较大,且两种物质的溶解度均随温度降低而减小,所以t2℃时,分别用100 g水配制甲、乙的饱和溶液,再降温到t1℃,析出固体的质量:甲>乙,选项正确,故选A。

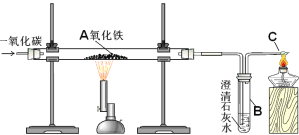
【题目】某兴趣小组的同学们在探究“可燃物燃烧的条件”时,通过查阅资料知:白磷的着火点是40℃,红磷的着火点是240℃,…燃烧产物五氧化二磷是白色固体,刺激人体呼吸道,吸入过量可引起中毒性肺炎.于是他们对装置甲进行了改进,如装置乙所示,a、b试管口均为胶塞.请按要求回答相关问题.
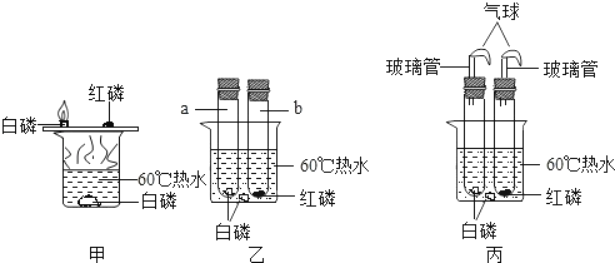
(实验操作)
(1)装置甲中白磷燃烧的化学方程式是_____.
(2)同学们按装置乙进行实验.请你版主他们完成下列表格.
观察到的现象 | 解释 |
a试管中白磷_____ 热水中白磷_____ | 热水中白磷产生这种现象的原因是_____ |
b试管中红磷_____ | B试管中红磷产生这种现象的原因是_____ |
(反思与评价)
(3)装置乙与装置甲比较,其优点是_____.
(4)有同学指出装置乙仍有不足之处,并设计了装置丙,其中气球的作用是:_____.
(拓展与迁移)
(5)实验室的化学药品不慎起火,常将沙土铺撒在燃烧的药品上,其作用是_____.
(6)保存少量白磷的方法是_____.
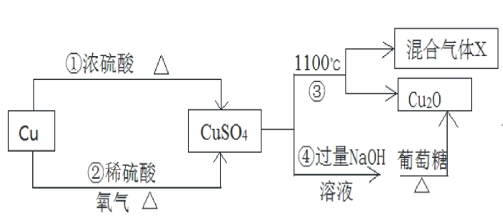
【题目】在化学实验室,某小组同学实验时发现一瓶没有密封好的 NaOH 已经结块。于是对其成分进行科学探究,请你一起完成探究的过程。
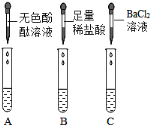
Ⅰ固体的成分分析
(提出问题)结块后的固体成分是什么?
(猜想与假设)
猜想一:固体为碳酸钠
猜想二:固体为碳酸钠和氢氧化钠。
用化学方程式表示固体中含有碳酸钠的原因______________
(查阅资料)BaCl2 溶液 pH=7。
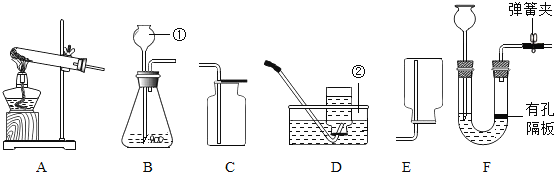
(实验探究)从瓶中取出一定量的固体,加入足量水溶解,再将溶液分三等份分别装入A、B、C 三支试管,进行如上图所示实验。
甲同学根据实验现象,认为结块固体中有碳酸钠和氢氧化钠。
(实验分析)
(1) 根据甲同学的实验结论可知,三支试管中观察到的实验现象分别为:A 试管中_______________________,B 试管出现大量气泡,C 试管中出现白色沉淀; C 试管中现象产生的原因是(用化学方程式表示)______________
(2)乙同学认为甲同学的结论是不正确的,原因是______________
(实验设计)请你设计合理的实验方案,填入下列表格中。
操作 | 现象 | 结论 |
取少量结块固体于试管(或烧杯)中, 加水使其完全溶解, ①______________ ②______________ | ①______________ ②______________ | 固体为碳酸钠和 氢氧化钠 |
Ⅱ 固体中各成分含量
为确定该固体样品中 Na2CO3 的质量分数,小芳同学称取 2 g 样品,利用 A 为 Y 形管、B为量气管、C 为水准管作为主要反应容器,进行了如图(I)所示实验。
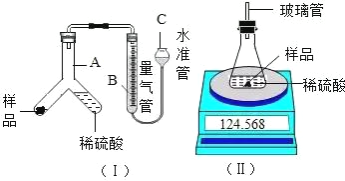
(1)在量气管内水面上加一薄层油,目的是______________
(2)使样品与稀硫酸反应的操作为______________
(3)实验结束后,小芳同学读出量气管中的气体体积为 22.4ml(已知该温度压强下,CO2的密度为 1.965 g/L),请你计算出样品中 Na2CO3 质量分数______________。(写出计算过程)
(4)小明同学设计如图(Ⅱ)装置,分别测定反应前、反应后仪器以及仪器内物质的总质量,进行有关计算,实验操作中没有失误,多次测量的结果均偏大,你认为可能的原因是______________