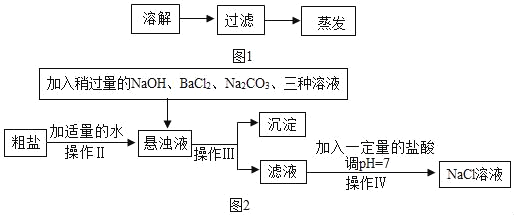
题目内容
【题目】下列图象能正确反映对应变化关系的是( )
|
|
|
|
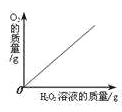
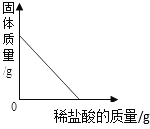
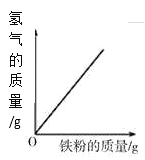
A.向一定量的二氧化锰中加入过氧化氢溶液 | B.将铁钉加入硫酸铜溶液中 | C.向一定量的大理石(杂质不参加反应)中加入足量的稀盐酸 | D.向一定质量的稀盐酸中加入足量铁粉 |
A. A B. B C. C D. D
【答案】A
【解析】
试题结合具体反应,对应图像分析。
A、向一定量的二氧化锰中加入过氧化氢溶液,过氧化氢在二氧化锰的催化作用下,分解产生水和氧气,由于氧气是生成物,故其质量随反应物过氧化氢的不断加入,会从0开始不断变大,正确;
B、将铁钉加入硫酸铜溶液中,二者发生置换反应生成铜和硫酸亚铁,即Fe+CuSO4="Cu+" FeSO4,其中参加反应的Fe与生成的Cu的质量比为56:64,由此可知,固体的质量随铁钉的加入而变大,图像正好相反,错误;
C、向一定量的大理石中加入足量的稀盐酸,二者反应生成氯化钙、水和二氧化碳,由此可知,固体的质量随盐酸的加入而变小,直至大理石完全反应,但由于其中的杂质不参加反应,故最终固体的质量不可能为0,错误;
D、向一定量的稀盐酸中加入足量的铁粉,二者发生置换反应生成氯化亚铁和氢气,即Fe+2HCl=FeCl2+H2↑,由于氢气是生成物,故其质量随反应物铁粉的不断加入,会从0开始不断变大直至盐酸完全反应不再变化,错误。故选A

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案【题目】某中学化学兴趣小组通过实验测定某大理石中碳酸钙的质量分数,将盛有20.0g该样品的烧杯放在电子秤上,倒入100.0g稀盐酸(假设大理石样品中的杂质不与稀盐酸反应,也不溶于水),使该样品恰好完全反应,实验过程中的有关数据如下表所示:
时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
烧杯与所盛物质质量/g | 174.0 | 171.0 | 169.0 | 168.0 | 167.4 | 167.4 |
计算:
(1)生成二氧化碳的质量;
(2)该大理石中碳酸钙的质量分数;
(3)反应完成所得溶液中溶质的质量分数(精确到0.1%)
【题目】(科学探究)
很多同学都喜欢既别致又实用的“树叶书签”,实验小组尝试制作了书签,并对该制作过程及所用试剂进行了研究。

Ⅰ.制作“树叶书签”
小组同学首先选取了大小适当的树叶,洗净后放在一定浓度的氢氧化钠溶液中煮沸,再加以处理,除去表皮和叶肉,只剩余清晰的叶脉,取出,冲洗,将叶片压平,最后系上各色丝带,漂亮的“叶脉书签”便做好了。
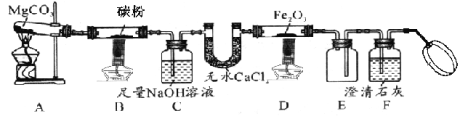
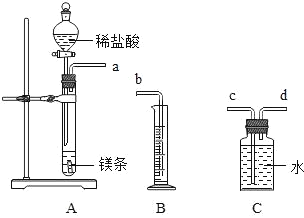
(1)小组同学用如图所示的装置煮沸树叶,指出其中的一处错误:_____。
Ⅱ.探究制作“叶脉书签”的最佳条件
(实验1)相同煮沸时间内,将洗干净的树叶放在不同浓度的氢氧化钠溶液里,处理后叶片变化如下表。
NaOH溶液浓度 | 1% | 5% | 10% |
叶片变化 | 留有很多叶肉 | 留有较多叶肉 | 残留很少叶肉 |
(实验2)在10%的氢氧化钠溶液里,将洗干净的树叶在不同温度下,进行煮沸,随着时间的变化,叶片变化如下表。
时间 叶片变化 温度 | 5min | 15min | 20min |
60℃ | 无明显变化 | 留有较多叶肉 | 留有少量叶肉 |
80℃ | 留有较多叶肉 | 留有少量叶肉 | 残留很少叶肉 |
100℃ | 留有较多叶肉 | 残留很少叶肉 | 叶片卷起来,叶肉与叶脉不易分离 |
(2)实验小组同学选择了10%的氢氧化钠溶液制作“叶脉书签”,原因是_____。
(3)通过实验2可知,制作“叶脉书签”的最佳加热的温度和时间是_____(写一种即可)。
Ⅲ.小组同学发现所用的氢氧化钠溶液瓶口有白色固体出现,这瓶溶液中的溶质只有氢氧化钠吗?同学们展开了下面的探究:
(4)氢氧化钠溶液放置在空气中可能发生的反应的化学方程式为_____。
同学们经过思考、讨论,分别设计了以下两个实验方案:
方案Ⅰ:打开瓶塞,取出少量溶液,并向其中加入少量稀盐酸,若未观察到有气泡产生,证明溶液没有变质。
方案Ⅱ:打开瓶塞,取出少量溶液,并向其中加入CaCl2溶液,若未观察到有白色沉淀产生,证明溶液没有变质。
(5)你认为上述实验方案不可行的是_____,理由是_____。
(6)同学们利用可行的方案进行实验,检验出该氢氧化钠溶液确实已变质,提出使用或保存氢氧化钠溶液的注意事项:_____(写出一点即可)。