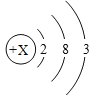��Ŀ����
����Ŀ��ʵ���ҳ��ù���������Һ�Ͷ�����������������ȡ������
��������⡿�����������̵������Է�Ӧ�����Ƿ���Ӱ�죿
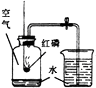
�����ʵ�顿��1��ʵ��װ����ͼ��ʾ��


![]() ��2��ʵ���¼��ʵ���������±���
��2��ʵ���¼��ʵ���������±���
�������������ml�� | ��������Ũ�� | ��������������g�� | ����������ml�� | |
�� | 30 | 5�� | 0.1 | |
�� | 30 | 5�� | 0.2 | |
�� | 30 | 5�� | 0.3 |
��ʵ���������1����������ֽ�����ֱ���ʽΪ____________________���������̿���Ϊ�÷�Ӧ�Ĵ�����������__________________��
��2�������еġ��������ݡ��ǣ���ͬʱ����_______________________
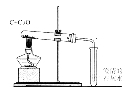
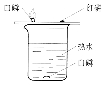
��3����ʵ���У��ⶨ�������ݵ�װ������ͼ�����߿�������_______����������
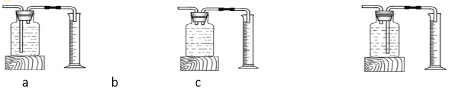
��4�����ڢ�αȵڢ��ʵ��ġ��������ݡ���______�����С����˵������������Խ�࣬��Ӧ���졣
��ʵ�鷴˼�������������ػ�Ӱ���������ķ�Ӧ�����⣬_________��дһ����Ҳ��Ӱ���������ķֽⷴӦ���ʣ���д�����ʵ�鷽����_______________________
���𰸡���1����������![]() ˮ+�������ܼӿ��������ķֽ����ʣ��������������ͻ�ѧ�����ڷ�Ӧǰ�����ռ����������
ˮ+�������ܼӿ��������ķֽ����ʣ��������������ͻ�ѧ�����ڷ�Ӧǰ�����ռ����������
��2��C��С����������Ũ����1����������ȡ��ͬ�������ͬŨ�ȵĹ���������Һ���ֱ������ͬ�����Ķ������̣��Ƚ���ͬʱ�����ռ����������Ӱ���������ֽ����ʵ����ػ��д������ࡢ�����Ŀ�����С����Ӧʱ���¶ȵȣ�������ѭ���Ʊ��������ɡ���
��������
������������������ڶ������̵������·ֽ�����ˮ�����������ж������̵������Ǽӿ��������ķֽ����ʣ�����Ӧǰ��������̵������ͻ�ѧ���ʲ��䣬�����ǹ�������ֽ�Ĵ������ȽϷֽ����ʵķ����ǣ��Ƚ���ͬʱ�������������Ķ��٣�װ��C�������Ӷ̹ܽ��룬Ȼ�����������ࡢѹ������ˮ�ӳ���ѹ����Ͳ�ڣ�������Ͳ�ڵ�ˮ����������ռ��������������ABװ�������ܴӶ̹ܳ�ȥ�����ܴﵽ�ռ������Ŀ�ģ����ڢ�αȵڢ��ʵ��ġ��������ݡ�����˵������������Խ�࣬��Ӧ���졣�¶ȡ����������Ũ�ȣ�����������ȶ���Ӱ���������ķ�Ӧ���ʣ�

����Ŀ�����ࡢ����dz��л�ѧ���õ�ѧϰ������
��1����ѧʵ��ɰ�����ҪĿ�ķ�Ϊ�����ʷ�����ѧ��Ӧ������̽�����������ʵ�̽�������ʺ�����̽���ȡ��ݴ�Ӧ������ʵ����D�� (�A���� ��B���� ��C��)��Ϊһ�࣬���ݵ�ʵ��Ŀ���� ��
A |
|
C |
D |
��2����������ԭ��Ӧ�У�Ԫ�ػ��ϼ����ߵķ�Ӧ��Ϊ��ԭ������֮Ϊ��������������ʵ��B�У��������� ����д����һ�ֵ��ʺ�һ�ֻ���������Ϸ�Ӧ�Ļ�ѧ����ʽ �����е���Ϊ��ԭ����������Ϊ����������