题目内容
【题目】实验兴趣小组对制取二氧化碳实验中剩余的滤液产生了浓厚的兴趣,已知在实验过程中加入的稀盐酸过量,溶质只含有氯化钙和氯化氢两种物质,为了探究各成分的质量进行了如下的实验。请回答下列问题:
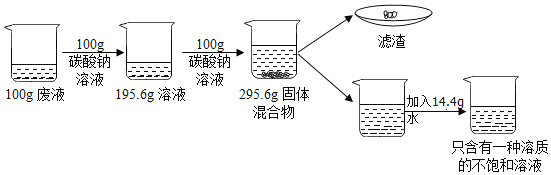
(1)写出生成气体的化学反应方程式_____。
(2)写出求解溶液中氯化氢质量(x)的比例式为_____。
(3)滤渣的质量为_____。
(4)第一次加入碳酸钠溶液的质量至50g时溶液中溶质的成分_____(填化学式)。
(5)最终所得不饱和溶液中溶质的质量分数为_____。
【答案】Na2CO3+2HCl═2NaCl+H2O+CO2↑ ![]() 10g NaCl、HCl、CaCl2 7.8%
10g NaCl、HCl、CaCl2 7.8%
【解析】
(1)碳酸钠和盐酸反应生成水和二氧化碳、氯化钠,化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(2)设溶液中氯化氢质量为x,反应生成氯化钠质量为y,溶液中碳酸钠的质量为z,反应生成二氧化碳质量为:100g+100g﹣195.6g=4.4g,
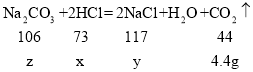
![]()
x=7.3g,y=11.7g,z=10.6g,
(3)第一次加入碳酸钠溶液没有沉淀生成并且溶液反应后总量减少,说明滤液中含有盐酸,第二次加入碳酸钠溶液有固体生成说明碳酸钠与氯化钙反应生成了碳酸钙沉淀,设生成碳酸钙的质量为m,生成氯化钠的质量为n,

![]() ,
,
m=10g,n=11.7g,
所以滤渣的质量为10g;
(4)加入100g的碳酸钠溶液,恰好完全反应,所以第一次加入碳酸钠溶液的质量至50g时,盐酸有剩余,溶液中溶质的成分是NaCl、HCl、CaCl2;
(5)最终所得不饱和溶液中溶质的质量分数为:![]() ×100%=7.8%。
×100%=7.8%。

【题目】分类、类比、推理都是学习化学常用的方法。
(1)物质的性质很大程度上决定了物质的用途,熟知物质的性质才能更好的应用物质,下图为初中化学教材中的实验。请回答问题:
A组 | B组 | 实验C | ||
石墨导电实验 |
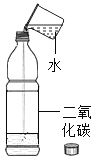
二氧化碳的溶解性实验 |
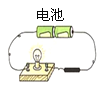
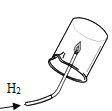
氢气燃烧 |
生石灰中加入水 |
酸或碱的溶液改变花的颜色 |
若按照研究物质性质的角度进行分类,应将实验C归为_____组,理由是_____;
(2)通过课外阅读发现有下列反应:
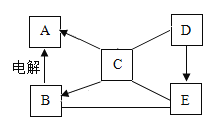
Cl2+2NaBr=2NaCl+Br2 Br2+2KI=2KBr+I2
Cl2 Br2 I2 是氯、溴、碘三种元素组成的三种非金属单质。经过类比分析,发现非金属单质与盐发生的置换反应跟金属与盐发生的置换反应有类似的规律。因此可以判断Cl2 Br2 I2 三种非金属中活泼性最强的是_____(写化学式)。
查阅资料又得知结论:硫的活泼性比上述三种单质的活泼性都弱。请仿照上述反应,用硫元素和钾元素组成的化合物与其发生的一个反应来证明此结论(用化学方程式回答)_____。