题目内容
【题目】已知草酸(H2C2O4)固体与浓硫酸共热发生化学反应:H2C2O4![]() CO2↑+CO↑+H2O.某化学兴趣小组设计如下实验装置,用于制取纯净干燥的CO气体来还原氧化铁。请根据题目要求回答下列问题:
CO2↑+CO↑+H2O.某化学兴趣小组设计如下实验装置,用于制取纯净干燥的CO气体来还原氧化铁。请根据题目要求回答下列问题:
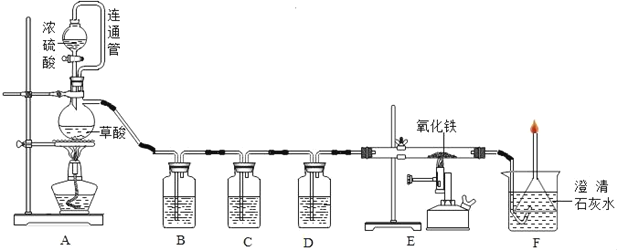
(1)按装置图组装好实验仪器,实验前必须要_____,点燃E处酒精灯前必须_____。
(2)装置B中的试剂是_____溶液,反应的化学方程式为_____;装置C中所盛的液体是_____,其作用是_____;
(3)E装置玻璃管中观察到的现象是_____,反应的化学方程式为_____;
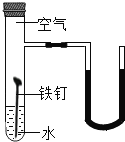
(4)A装置中连通管的作用是_____;
(5)F装置的作用是_____、_____(只答二条即可);
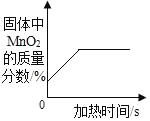
(6)利用这套装置还可以测定氧化铁样品中氧化铁的质量分数。某同学的测定方法是:称量氧化铁样品10.0 g,E装置中玻璃管与样品的总质量为80.0 g,完全反应并冷却后再称量E装置中玻璃管与剩余固体的总质量为78.2 g.由该实验可计算出氧化铁样品中氧化铁的质量分数为_____。
【答案】检查装置的气密性 检验气体的纯度 浓氢氧化钠 2NaOH+CO2=Na2CO3+H2O 澄清的石灰水 检验混合气体中的二氧化碳是否除尽 红色粉末逐渐变为黑色 Fe2O3+3CO![]() 2Fe+3CO2 使支管烧瓶与分液漏斗内气体压强相同,便于滴入酸液 检验生成物中是否含有二氧化碳 收集尾气中的一氧化碳,将其点燃转化为无毒的二氧化碳 60%
2Fe+3CO2 使支管烧瓶与分液漏斗内气体压强相同,便于滴入酸液 检验生成物中是否含有二氧化碳 收集尾气中的一氧化碳,将其点燃转化为无毒的二氧化碳 60%
【解析】
(1)该实验过程中有气体生成、有气体参加,所以按装置图组装好实验仪器,实验前必须要检查装置的气密性;一氧化碳具有可燃性,点燃不纯的一氧化碳或加热易发生爆炸,所以点燃E处酒精灯前必须检验气体的纯度;
(2)该实验要制取纯净干燥的CO气体来还原氧化铁,而生成的气体中含有一氧化碳、二氧化碳和水蒸气,所以B装置内是浓氢氧化钠溶液,氢氧化钠溶液与二氧化碳反应生成碳酸钠和水,2NaOH+CO2=Na2CO3+H2O,其作用是除去气体中的二氧化碳;C装置中是澄清石灰水,用于检验混合气体中的二氧化碳是否除尽;
(3)在高温的条件下,一氧化碳与氧化铁反应生成铁和二氧化碳,Fe2O3+3CO![]() 2Fe+3CO2,氧化铁是红色粉末状固体,生成的铁因含有杂质而呈现黑色,所以可观察到玻璃管内的红色粉末慢慢变成黑色;
2Fe+3CO2,氧化铁是红色粉末状固体,生成的铁因含有杂质而呈现黑色,所以可观察到玻璃管内的红色粉末慢慢变成黑色;
(4)由于实验一般在密闭环境下进行,滴入一定液体后会发生内外压不平衡情况,此时液体就不易滴下,采用连通管可平衡内外压帮助液体顺利滴下;
(5)F装置既可以检验生成物中是否含有二氧化碳,还能收集尾气中的一氧化碳,将其点燃转化为无毒的二氧化碳。
(6)设氧化铁的质量为x,则:
![]()
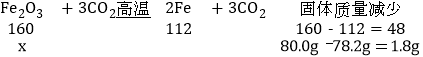
![]() =
=![]() ,解得x=6g
,解得x=6g
氧化铁样品中氧化铁的质量分数为:![]() ×100%=60%
×100%=60%

 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案