题目内容
【题目】小明同学用下图总结了NaOH的化学性质(即NaOH与四类物质都能够发生化学反应)。

⑴反应③属于____________(填写基本反应类型)
⑵为了验证反应④能够发生,你选择的物质是___________。
A.Na2CO3 B.HCl C.CuSO4 D.NaCl
⑶依据反应②说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为:__________。
【答案】 复分解反应 C 2NaOH+CO2=Na2CO3+H2O
【解析】(1)反应③是酸与碱反应生成盐和水,故是复分解反应;
(2)A、碳酸钠和氢氧化钠互相交换成分后不能生成气体、沉淀和水,故碳酸钠和 氢氧化钠不能反应;B、HCl不是盐,故错误;C、CuSO4可以与氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,故正确;D、氯化钠与氢氧化钠交换成分后不能生成气体、沉淀或水,故错误。故选C。
(3)氢氧化钠易与空气中的二氧化碳反应变质,故要密封保存,氢氧化钠与二氧化碳反应生成碳酸钠和水,反应方程式为2NaOH+CO2=Na2CO3+H2O。

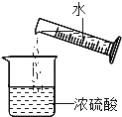
【题目】图一、图二是某兴趣小组探究金属、酸的化学性质时所做的两组实验。实验结束后,将两组实验试管中的物质分别全部倒入甲、乙两个洁净的烧杯中,据图回答:
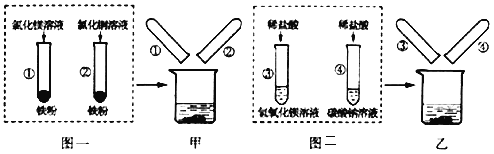
(1)在图一所示的实验中,试管②中发生反应的化学方程式是_____。
(2)甲烧杯中的物质完全反应后,发现红色固体物质明显增多。下列说法正确的是_____(填序号)
A.试管②反应后的固体中一定不含铁
B.完全反应后,甲烧杯中的固体一定含有铁
C.完全反应后,甲烧杯的溶液中可能含有Cu2+
D.完全反应后,甲烧杯的溶液中一定含有Mg2+、Fe2+
(3)乙烧杯中的物质充分反应后,仅观察到有白色沉淀,无其他现象。则试管④反应后的溶液中的溶质共有哪些_____(写化学式)。
(4)将乙烧杯内的物质进行过滤,对所得滤液中溶质成分进行了如下探究:
实验操作 | 实验现象 | 实验结论 |
步骤1:取少量滤液于试管中,向其中滴加足量硝酸钡溶液, | 有白色沉淀生成 | ①生成的白色沉淀是_____(写化学式,下同) ②滤液中的溶质共有哪些_____ |
步骤2:静置,向上层清夜中滴加无色酚酞试液 | 溶液变红 |
(5)在上述(4)的实验探究中,步骤1中加入足量硝酸钡溶液的目的是_____。
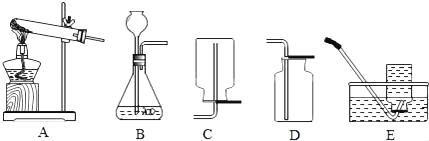
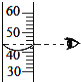
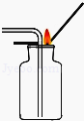
【题目】根如据图所示装置完成实验,并按要求填写表格内容。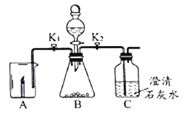
关闭K2打开K1A中现象 | B中发生反应化学方程式 | 解释A中现象 | 关闭K1打开K2C中现象 | 用化学方程式解释C中现象 |
蜡烛熄灭 | ______ | _____ | _____ | _____ |
蜡烛燃烧更旺 | _____ | ______ | _____ |