题目内容
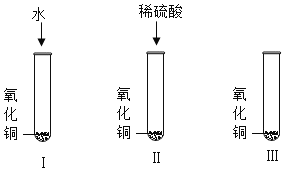
【题目】氧化铜是一种黑色固体,可溶于稀硫酸,某同学想知道是稀硫酸中的哪种粒子(H2O、H+、S![]() )能使氧化铜溶解。请你和他一起通过图中Ⅰ、Ⅱ、Ⅲ三个实验完成这次探究括动。下列说法错误的是( )
)能使氧化铜溶解。请你和他一起通过图中Ⅰ、Ⅱ、Ⅲ三个实验完成这次探究括动。下列说法错误的是( )
A. 不做实验Ⅰ也能说明H2O不能使CuO溶解
B. 在Ⅲ中应该加入盐酸
C. 此实验说明稀硝酸也能溶解氧化铜
D. 可以提出的假设溶液中的H+使CuO溶解
【答案】B
【解析】
由实验的图示可知I是验证水能否溶解氧化铜,II则是加入稀硫酸,加入的实际是两种离子,氢离子和硫酸根离子,所以III应该是加入含有硫酸根的物质。
A.不做I实验II、III中只要是加入溶液,则就有水参与的反应出现,分析知III可以是加入硫酸钠的溶液,而氧化铜没有溶解,可以说明 H2O 不能使 CuO 溶解,故A说法正确;
B、分析知III应该是加入含有硫酸根的物质,不应该加入盐酸,故说法错误;
C、该实验的目的是验证氢离子溶解氧化铜,而稀硝酸中含有氢离子,所以稀硝酸也能溶解氧化铜,故说法正确;
D、由于实验的目的是稀硫酸中的哪种粒子(H2O、H+、SO42-)能使氧化铜溶解,所以可以提出的假设溶液中的 H+使 CuO溶解,故说法正确。
故选:B。

 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案【题目】化学兴趣小组的同学探究金属和盐溶液反应时,发现将钠放入![]() 溶液中有气泡和白色沉淀产生。为了进一步探究,小组同学将充分反应后的混合物过滤,得固体A和滤液B。
溶液中有气泡和白色沉淀产生。为了进一步探究,小组同学将充分反应后的混合物过滤,得固体A和滤液B。
![]() 查阅资料)钠与水反应生成氢氧化钠和氢气
查阅资料)钠与水反应生成氢氧化钠和氢气
(分析、思考、实验)钠放入![]() 溶液中产生的气泡,应该是______;取固体A加入过量稀盐酸,A全部溶解,且无气泡产生,此反应的化学方程式为______;
溶液中产生的气泡,应该是______;取固体A加入过量稀盐酸,A全部溶解,且无气泡产生,此反应的化学方程式为______;
提出问题)滤液B中的溶质成分是什么?
(提出猜想)猜想![]() :有
:有![]() 和NaOH猜想
和NaOH猜想![]() :有
:有![]() 和
和![]()
猜想![]() :______;
:______;
(实验设计)
实验操作 | 实验现象或发生反应的方程式 | 实验结论 |
方案一:取滤液B少许于试管中,滴入硫酸铜溶液 | 无明显现象 | 猜想 |
方案二:取滤液B少许于试管中,滴入氢氧化钠溶液 | 方程式为:______ | 猜想 |
方案三:取滤液B少许于试管中,滴入氢氧化钡溶液 | 现象为:______ | @@@/ |
(讨论交流)通过讨论大家一致认为方案三不可取,原因是______。
【题目】一定条件下,下列物质在密闭容器内反应。一段时间后,测得反应前后各物质的质量如表所示,其中A的相对分子质量是18,B的相对分子质量是2。
物质 | A | B | C | D |
反应前质量/g | 57 | 4 | 8 | 9 |
反应后质量/g | 21 | 待测 | 8 | 41 |
则反应后B的质量为______;该反应中B和D两种物质变化的质量比为______;该反应中A和B两种物质的化学计量数之比是______;
【题目】在学习盐的性质时,老师从实验室带来一瓶标签破损的溶液M![]() 如图
如图![]() 。
。
探究一:溶液M的溶质是什么?
(猜想与假设)
![]() 同学们认为溶液M的溶质可能是
同学们认为溶液M的溶质可能是![]() 或______
或______![]() 写化学式
写化学式![]()
(实验探究)同学们进行了如下探究:
实验操作 | 实验现象 | 实验结论 |
取溶液M于试管中,滴加无色酚酞溶液 | ______ | 溶液M的溶质不是 |
探究二:老师取一定量溶液M与碳酸钠溶液混合,有白色沉淀产生,过滤后得到澄清滤液,滤液中的溶质成分是什么?
(猜想与假设)甲、乙、丙三位同学对溶质的成分做出如下猜想:
甲同学的猜想:NaCl、![]()
乙同学的猜想:NaCl、![]()
丙同学的猜想:NaCl
(分析与讨论)![]() 同学们一致认为同学的猜想不正确,理由是______。
同学们一致认为同学的猜想不正确,理由是______。
(实验验证)甲同学为了证明自己的猜想,进行了如下实验:
实验操作 | 实验现象 | 实验结论 | 分析判断 |
取样于试管中,加入硝酸银溶液 | 有白色沉淀产生 | 自己的猜想正确 | 该实验结论 ______ |
(总结与交流)![]() 甲同学加入硝酸银溶液后,溶液中一定含有的离子是______
甲同学加入硝酸银溶液后,溶液中一定含有的离子是______![]() 填离子符号
填离子符号![]() 。同学们通过合作探究,最终确定了溶质的成分。
。同学们通过合作探究,最终确定了溶质的成分。
(反思与收获)![]() 由上述探究可知,若想证明反应所得溶液溶质成分的某种猜想是否成立,一般思路是:证明______。思路明确后,再选取合适的试剂,最终才能得出实验结论。
由上述探究可知,若想证明反应所得溶液溶质成分的某种猜想是否成立,一般思路是:证明______。思路明确后,再选取合适的试剂,最终才能得出实验结论。