��Ŀ����
����Ŀ����������Na2CO3��Һ���뵽һ����CuSO4��Һ�еõ���ɫ���塣ij�о���ѧϰ
С�����ɫ����ijɷֽ���������̽������������и��⣺
��һ����������裺
����һ������ΪCuCO3�����ɣ� ���û�ѧ��Ӧ����ʽ��ʾ����
�����������ΪCu(OH)2�����ɣ�Na2CO3��Һ�� ����ᡱ����ԡ�
������������ΪCu(OH)2��CuCO3�Ļ���
���������ϲ��ģ�
��Cu(OH)2��CuCO3����������ᾧˮ��
��Cu(OH)2��CuCO3�����ֽ⣬�����ɶ�Ӧ�����������
�����������ʵ�飺
����Ļ�ȡ��
��1������Ӧ��Ĺ̡�Һ����ᆳ ��ϴ�ӡ����º�ɵ���ɫ���塣
��2���жϹ�����ϴ���ķ��������� ��
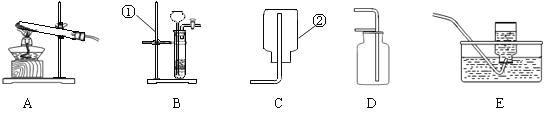
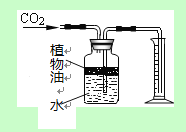
������ͼ��ʾװ�ã�����̽������ijɷ֡�

��3������װ��A��B��Ͻ���ʵ�飬B������������� ��ȷ��
��4������װ��A��C��Ͻ���ʵ�飬C������������� ��ȷ��
��5��С��ͬѧ��װ�ð� A�� �� ���B������C������˳����Ͻ���ʵ�飬��֤������������ȷ�ģ�ʵ���У�B�е�����Ϊ ��
C�е�����Ϊ ��
���ۣ�����ΪCu(OH)2��CuCO3�Ļ���
����ɷֶ����ⶨ��
��֪Cu(OH)2�ķֽ��¶�Ϊ66���68����CuCO3�ķֽ��¶�Ϊ200����220�������������ΪaCu(OH)2bCuCO3��С��ͬѧ���ȷ����ǶԹ�������ȷֽ⣬���������ݣ���ɹ��������仯��ֽ��¶ȵĹ�ϵ����ͼ�������ͼʾ�ش��������⣺
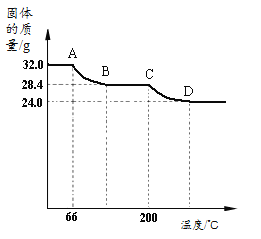
��6��д��A B��C D�η�����Ӧ�Ļ�ѧ����ʽ��
AB�� ��
CD�� ��
��7��ͨ������ɵã� a:b�� ��
��8������24.0gʣ�����������ȵ����ߵ��¶ȣ����ֹ�������������2.4g���������ٸı䣬д���˹����п��ܷ�����Ӧ�Ļ�ѧ����ʽ�� ��
���𰸡�����һ��Na2CO3 + CuSO4= CuCO3��+ Na2SO4����������1�� ���ˣ�2��ȡ���ϴ��Һ�������μ�������ϡ���ᣨ���ᡢ���ᣩ�������ݲ�������μ�BaCl2[��Ba(OH)2��Ba(NO3)2]��CaCl2[��Ca(OH)2��Ca(NO3)2]��Һ������������
��3������4��һ��5��CB�������ʯ��ˮ����ǣ���ɫ���������6��Cu(OH)2![]() CuO+H2O��CuCO3
CuO+H2O��CuCO3![]() CuO+CO2����7��2:1��8��4CuO
CuO+CO2����7��2:1��8��4CuO![]() 2Cu2O+O2��
2Cu2O+O2��
��������
�����������������Na2CO3��Һ���뵽һ����CuSO4��Һ�еõ���ɫ���塣��������裺����һ������ΪCuCO3�����ɣ�Na2CO3+CuSO4=CuCO3��+Na2SO4�������������ΪCu(OH)2�����ɣ�Na2CO3��Һ�ʼ��ԡ�������������ΪCu(OH)2��CuCO3�Ļ�������Ӧ��Ĺ̡�Һ����ᆳ������ϴ�ӡ����º�ɵ���ɫ���塣�жϹ�����ϴ���ķ���������ȡ���ϴ��Һ�������μ�������ϡ���ᣨ���ᡢ���ᣩ�������ݲ�������μ�BaCl2[��Ba(OH)2��Ba(NO3)2]��CaCl2[��Ca(OH)2��Ca(NO3)2]��Һ����������������װ��A��B��Ͻ���ʵ�飬B�����������������ȷ������װ��A��C��Ͻ���ʵ�飬C�������������һ��ȷ��С��ͬѧ��װ�ð�A��C��B��˳����Ͻ���ʵ�飬������Ҫ�ȼ���ˮ�IJ������ڼ��������̼�IJ�������֤������������ȷ�ģ�ʵ���У�B�е�����Ϊ�����ʯ��ˮ����ǣ���C�е�����Ϊ��ɫ���������AB�Σ�Cu(OH)2![]() CuO+H2O�����������û�м��٣�CD�Σ�CuCO3
CuO+H2O�����������û�м��٣�CD�Σ�CuCO3![]() CuO+CO2�����⣺����ͼ�ɵ�AB����Cu(OH)2���ȷֽ⣬���ɵ�ˮ������Ϊ32.0g��28.4g=3.6g
CuO+CO2�����⣺����ͼ�ɵ�AB����Cu(OH)2���ȷֽ⣬���ɵ�ˮ������Ϊ32.0g��28.4g=3.6g
������3.6gˮ�����Cu(OH)2������Ϊ![]() ��
��
Cu(OH)2![]() CuO+H2O
CuO+H2O
98 18
![]() 3.6g
3.6g
�б���ʽ�ã�98��X=18��:36�ˣ����X=19.6�ˣ�
����CuCO3������Ϊ32.0g��19.6g =12.4g
������ɫ������ɿɵ�98a��124b=19.6�ˣ�12.4�� ��a��b=2��1
����24.0gʣ�����������ȵ����ߵ��¶ȣ����ֹ�������������2.4g���������ٸı䣬�˹����п��ܷ�����Ӧ�Ļ�ѧ����ʽ��4CuO ![]() 2Cu2O + O2 ����
2Cu2O + O2 ����

 ��У����ϵ�д�
��У����ϵ�д�