��Ŀ����
����Ŀ����ѧ��һ����ʵ��Ϊ�����Ŀ�ѧ�� �����dz��л�ѧʵ���г�����ʵ��װ�á���ͬѧ��������Щװ�������п��ֵ�ʵ��̽����!
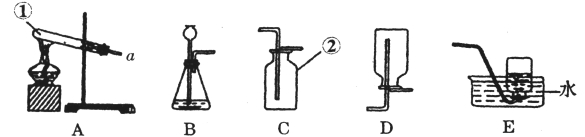
��1������д��ָ���������ƣ���__________����_____________��
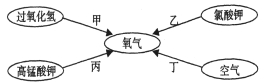
��2����ͼ��ʾ����;�������Եõ�����
��д��ʵ������ͨ����;����ȡ�����Ļ�ѧ����ʽ��_________ ___��
�ڻ�ѧʵ�����ɫ��������ɫ��ѧ�������ԭ����ָ��ʵ�鹤������ʵ��ԭ�Ϻͷ�Ӧ���̵���ɫ�����ǣ�����Ϊ�ڳ��л�ѧʵ�����У��ס��ҡ���������ȡ������;���У�__________(��ס�������"����;�������ֻ�ѧʵ�����ɫ����
��3��ʵ�����ø��������ȡ����ʱ����ѡ�õķ���װ����____________(����ĸ����)������ˮ���ռ�������Ϻ�Ӧ���еIJ���˳������______________��Ȼ��________________���Է�ֹˮ�������ȵ��Թ��У�����Թ�ը�ѡ�
��4��ʵ������ȡ������̼ʱ����ѡ�õķ���װ���� (����ĸ����)��д���÷�Ӧ��ѧ����ʽ ���ռ�������̼ͨ����Cװ�ã�����ѡ��D��Eװ�ã��ԴӶ�����̼���ʵĽǶ���������ԭ�� ��������Cװ���ռ�������̼�ķ��� ��
���𰸡���1���Թ� ����ƿ��2�� 2KClO3![]() 2KCl + 3O2�� �ף�3��A ��ˮ���еĵ����Ƴ�ˮ�� ֹͣ���� ��4��B CaCO3+2HCl==CaCl2+CO2��+H2O ������̼�ܶȱȿ�����������ˮ ��ȼ�յ�Сľ������ƿ��
2KCl + 3O2�� �ף�3��A ��ˮ���еĵ����Ƴ�ˮ�� ֹͣ���� ��4��B CaCO3+2HCl==CaCl2+CO2��+H2O ������̼�ܶȱȿ�����������ˮ ��ȼ�յ�Сľ������ƿ��
��������
�����������1����Ϊ�Թܣ���Ϊ����ƿ ��2��������غͶ��������ڼ��ȵ������£������Ȼ��غ��������ڴ�ʵ��ԭ�Ϻͷ�Ӧ���̵���ɫ�����ǣ�Ӧѡ���;�������ֻ�ѧʵ�����ɫ��3�����ݷ�Ӧ��״̬�ͷ�Ӧ��������֪ѡ��̹̼����ͷ���װ�ã���A������ˮ���ռ�������ʵ�����ʱӦ�Ƚ����ܴ�ˮ����ȡ������Ϩ��ƾ��ơ���4��ʵ������ȡ������̼Ӧѡ���Һ�����ͷ���װ�ã���Ӧ�Ļ�ѧ����ʽΪ��CaCO3+2HCl==CaCl2+CO2��+H2O ���ռ�������̼Ӧ���������ſ���������Ϊ������̼�ܶȱȿ�����������ˮ����ˮ������Ӧ�����������̼�ռ����ķ����ǽ�ȼ�ŵ�Сľͷƽ���ڼ���ƿ�ڣ���СľͷϨ��֤�����ռ�����

 ״Ԫ����ϵ�д�
״Ԫ����ϵ�д� ͬ������ϵ�д�
ͬ������ϵ�д�����Ŀ�������̲��ŷḻ����Դ��̽��ѧϰС���Ժ���Ca2+��Mg2+��Cl����±ˮ�ͱ��ǣ���Ҫ�ɷ�ΪCaCO3��Ϊ��Ҫԭ����ʵ�����Ʊ���ˮCaCl2��������ͼ1��

��ش��������⣺
��1�����������õ��IJ����������ձ����������� ��
��2����MgCl2Ϊ��д��±ˮ�г�ȥMg2+ʱ������Ӧ�Ļ�ѧ����ʽ ��
��3���������ữʱӦѡ������� ����д��ѧʽ����
��4���������MgCl2�Ļ�ѧ����ʽ�� ����Ҫ��֤þ������ͭ�Ļ��˳��ѡ����˿��Ҫѡ�� �� ������Һ��
��5��Mg(OH)2���ȷֽ�����MgO��H2O��MgO�Ǹ��۵�Ļ����ijЩ��ȼ�����谭ȼ�յ����ʣ�����Ч�ɷ���Mg(OH)2������ΪMg(OH)2�ܹ���ȼ��ԭ������� ��ѡ����ţ�
a��Mg(OH)2�ֽ���Ҫ���մ������ȣ������˿�ȼ����Ż��
b�����ɵ�����þ�����ڿ�ȼ����棬�����˿���
c�����ɵ�ˮ���������˿�ȼ����Χ����Ũ��
d����Ӧ�����Ƚ����˻����¶ȣ�ʹ��ȼ�ﲻ�״ﵽ�Ż��
��6����������ͼ��δ�漰�Ļ�����Ӧ������ ����д��ĸ��ţ�
a�����ֽⷴӦ b���û���Ӧ c�����Ϸ�Ӧ d���ֽⷴӦ
����֪T��ʱ���ֻ�������ˮ�к�Һ���е��ܽ�����±���
AgNO3 | Ba(NO3)2 | AgCl | BaCl2 | |
H2O��1�� | 170g | 92.0g | 1.50��10��4g | 33.3g |
NH3��1�� | 86.0g | 97.2g | 0.80g | 0.00g |
����������������Һ���з������ֽⷴӦ�Ļ�ѧ����ʽΪ ��
�̻��յ�CO2������������ʹ�������������ˮ������Ӧ������CH4��O2���÷�Ӧ�Ļ�ѧ����ʽΪ ������������ʱ���ڲ�ͬ�������١��ڡ��ۣ��������£�CH4���������ʱ��ı仯��ͼ2��ʾ���ڵ�10СʱʱCH4��������� ����д���١������ڡ����ۡ�����
������[CO(NH2)2]�������ʳ����������Ҫ�����á����ǿ�����������ʹCO2������M������Ӧ��CO2+2M�TCO(NH2)2+H2O������M�Ļ�ѧʽΪ ����CO2ת����Ϊ90����������1����������CO2�������Ƕ��٣�д��������̡�



