题目内容
【题目】味精是生活中的调味品。味精的鲜味来自于主要成分“谷氨酸钠”(化学 式是C5H8NO4Na,易溶于水,与AgNO3不反应),另外还含有NaCl及其它成分。
(1)实验表明,味精在100 °C时加热半小时,只有0. 3%的味精(谷氨酸钠)生成焦谷氨酸钠(有毒),对人体的影响甚微。对此,下列认识正确的是________________________。
a 味精不能吃,对人体有害
b 尽量避免在菜肴温度较高时使用味精
c 生成焦谷氨酸钠的过程是物理变化
d 实验是研究问题的一种有效方法
(2)称取5.0 g味精配制成50 g溶液,量取蒸馏水的量筒规格是__________________。
a 10 mL b 50 mL c 100 mL
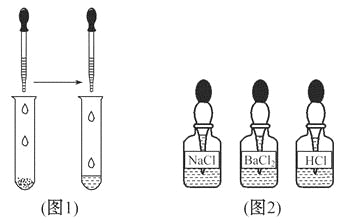
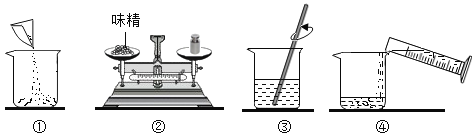
(3)如图是配制过程,正确的操作顺序为_________ (填序号)。
(4)为测定味精中NaCl的质量分数,进行如下实验:向上述配制好的溶液中加入AgNO3溶液至_______。反应的化学方程式是____。过滤后得沉淀质量为2.87 g,则该味精中NaCl的质量分数为______。
(5)实验后对比味精袋上的标签,发现所测得的NaCl的质量分数偏高,则可能的原因是____(填字母)。
a 配制溶液时仰视量水
b 反应中加入的AgNO3溶液过量
c 洗涤、干燥沉淀不彻底
d 味精中有其它能与AgNO3反应生成沉淀的物质
【答案】bd b ②①④③ 不再产生沉淀 NaCl+AgNO3═AgCl↓+NaNO3 23.4% cd
【解析】
(1)a.味精在100℃时加热半小时,只有0.3%的味精(谷氨酸钠)生成焦谷氨酸钠(有毒),对人体的影响甚微,因此味精能吃,该选项说法不正确;
b.尽量避免在菜肴温度较高时使用味精,这是因为味精在温度较高时容易变质,该选项说法正确;
c.生成焦谷氨酸钠的过程是化学变化,该选项说法不正确;
d.实验是研究问题的一种有效方法,该选项说法正确.
故填:bd.
(2)称取5.0g味精配制成50g溶液,量取蒸馏水的体积为:(50g-5.0g)÷1g/mL=45mL,因此应该选择50mL的量筒.
故填:b.
(3)如图是配制过程,正确的操作顺序为:称量、把称量的味精放入烧杯中、量取水倒入烧杯中、利用玻璃棒搅拌使味精溶解.
故填:②①④③.
(4)为测定味精中NaCl的质量分数,进行如下实验:向上述配制好的溶液中加入AgNO3溶液至不再产生沉淀,氯化钠和硝酸银反应生成氯化银沉淀和硝酸钠,反应的方程式为:NaCl+AgNO3═AgCl↓+NaNO3;
设氯化钠质量为x,

x=1.17g,
则该味精中NaCl的质量分数为:![]() ×100%=23.4%,
×100%=23.4%,
故填:不再产生沉淀;NaCl+AgNO3═AgCl↓+NaNO3;23.4%.
(5)a.配溶液时仰视量水,会导致水的体积偏大,从而导致配制溶液的质量分数偏小;
b.反应中加入的AgNO3溶液过量时,才能够使氯化钠完全反应,从而使计算结果正确;
c.洗涤、干燥沉淀不彻底时,会导致氯化钠质量偏大,从而导致计算结果偏大;
d、味精中有其它能与AgNO3反应生成沉淀的物质时,会导致氯化钠质量偏大,从而导致计算结果偏大.
故填:cd.

 阅读快车系列答案
阅读快车系列答案