题目内容
为了除去氯化钠样品中的碳酸钠杂质,某兴趣小组将样品溶解后进行如图实验:

请回答下列问题:
(1)将无色溶液与沉淀B分离的操作①的方法名称是 ,从无色溶液得到固体物质C的操作②的方法是 ,分析采用这种结晶方法的原因是 ;
(2)操作①中滴加过量的氯化钙溶液,则沉淀B的化学式为 ,无色溶液A中溶质是 ;
(3)为了既能除去杂质碳酸钠,又能有效地防止新杂质的引入,可向样品溶液中加入适量的稀盐酸,调节pH 7(填“>”、“<”或“=”),直接进行操作②即可得到纯净的氯化钠固体.写出有关反应的化学方程式为 .

请回答下列问题:
(1)将无色溶液与沉淀B分离的操作①的方法名称是
(2)操作①中滴加过量的氯化钙溶液,则沉淀B的化学式为
(3)为了既能除去杂质碳酸钠,又能有效地防止新杂质的引入,可向样品溶液中加入适量的稀盐酸,调节pH
考点:氯化钠与粗盐提纯,过滤的原理、方法及其应用,蒸发与蒸馏操作,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的盐 化学肥料
分析:(1)根据所要分离混合物的特点,判断流程中的操作方法;根据从溶液中获得晶体的操作方法和原理分析;
(2)根据样品溶液的组成,结合反应流程,分析沉淀B是什么物质;
(3)根据除去杂质的基本要求和所含碳酸根的性质,可选择碳酸根遇酸化气的方法,调节pH=7,碳酸钠都被反应,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳解答.
(2)根据样品溶液的组成,结合反应流程,分析沉淀B是什么物质;
(3)根据除去杂质的基本要求和所含碳酸根的性质,可选择碳酸根遇酸化气的方法,调节pH=7,碳酸钠都被反应,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳解答.
解答:解:(1)样品溶液中的碳酸钠与氯化钙反应能生成不溶性的碳酸钙,故沉淀B的化学式为 CaCO3,由于加入的是过量的氯化钙,故无色溶液A中溶质有 NaCl、CaCl2 ;
(2)加入氯化钙后生成了不溶于水的碳酸钙沉淀和氯化钠,要将沉淀分离出来,需要过滤,故操作①的名称是 过滤,无色溶液为氯化钠溶液和氯化钙溶液的混合物,要获得晶体需要采取蒸发结晶的操作,操作②的名称是蒸发;
(3)碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,二者恰好完全反应所得溶液是氯化钠的溶液,该溶液呈中性,pH=7,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
故答案为:(1)过滤;蒸发;这种固体溶质的溶解度受温度的影响不大;
(2)CaCO3;NaCl和CaCl2
(3)Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(2)加入氯化钙后生成了不溶于水的碳酸钙沉淀和氯化钠,要将沉淀分离出来,需要过滤,故操作①的名称是 过滤,无色溶液为氯化钠溶液和氯化钙溶液的混合物,要获得晶体需要采取蒸发结晶的操作,操作②的名称是蒸发;
(3)碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,二者恰好完全反应所得溶液是氯化钠的溶液,该溶液呈中性,pH=7,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
故答案为:(1)过滤;蒸发;这种固体溶质的溶解度受温度的影响不大;
(2)CaCO3;NaCl和CaCl2
(3)Na2CO3+2HCl═2NaCl+H2O+CO2↑.
点评:在做物质的除杂题时,要搞清除需要除去的离子,在选择适当的试剂将其沉淀,当加入的试剂的状态和杂质状态相同时,要注意加入量的控制.

练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
下列物质由合成材料制造的是( )
| A、纯棉衬衫 | B、玻璃 |
| C、钢筋混凝土 | D、塑料食品袋 |
下列物质性质的描述中,属于化学性质的是( )
| A、甲烷可以在空气中燃烧 |
| B、小苏打是白色粉末状晶体,能溶于水 |
| C、二氧化碳密度比空气大 |
| D、银是银白色固体,具有良好的延展性 |
下列变化中,只有一个变化与其他变化的本质是不同的,该变化是( )
A、 鲜奶制酸奶 |
B、 苹果腐烂 |
C、 菜刀生锈 |
D、 水果榨果汁 |
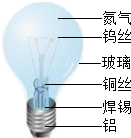 如图标出的是有关灯泡的组成,请根据图回答下列问题.
如图标出的是有关灯泡的组成,请根据图回答下列问题.