题目内容
【题目】了探究化学反应前后物质的总质量是否发生改变,甲同学和乙同学分别设计了下面两个实验,请根据图示回答问题:
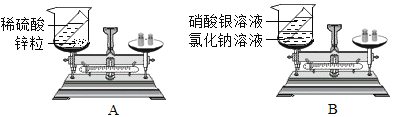
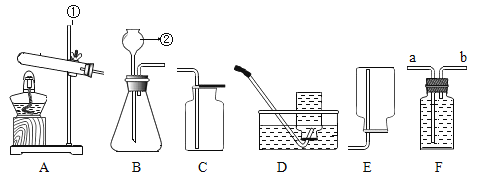
(1)甲同学设计的实验如图A所示,反应前,托盘天平的指针指向刻度盘的中间。两种物质反应后,托盘天平的指针_______(填“向左”“向右”或“不”)偏转,原因是_________
(2)乙同学设计的实验如图B所示,通过实验得出结论:化学反应前后物质的总质量_____。
(3)两位同学通过交流反思得到启示:____________
(4)从微观角度分析,在化学反应前后一定不变的是__________(填序号)。
①原子种类 ②分子种类 ③原子数目 ④分子质量 ⑤分子数目 ⑥原子质量
【答案】向右 反应生成的氢气逸出装置 相等 有气体参加的反应,验证质量守恒定律时要在密封容器中进行 ①③⑥
【解析】
(1)反应前,托盘天平的指针指向刻度盘的中间,两种物质反应后,托盘天平的指针向右偏转,原因是:锌和稀硫酸反应生成的氢气逸出装置外。
故填:向右;反应生成的氢气逸出装置。
(2)乙同学设计的实验如图B所示,硝酸银和氯化钠反应生成白色沉淀氯化银和硝酸钠,反应前后托盘天平的指针不发生偏转,说明化学反应前后物质的总质量相等。
故填:相等。
(3)通过交流反思得到启示:有气体参加的反应,验证质量守恒定律时要在密封容器中进行。
故填:有气体参加的反应,验证质量守恒定律时要在密封容器中进行。
(4)从微观角度分析,在化学反应前后:原子种类一定不变,分子种类一定改变,原子数目一定不变,生成的新的分子的分子质量可能改变,也可能不变,分子数可能改变,也可能不改变,原子质量一定不改变。
故填:①③⑥。

【题目】如图为实验室常见的气体制备、收集和性质的实验装置,据图回答。

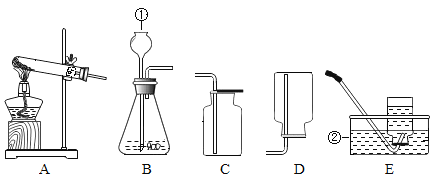
(1)指出B装置中标号仪器名称:①_____。
(2)实验室用大理石与稀盐酸反应制取CO2应选择的发生装置是_____(填装置序号,下同),收集装置是_____,反应的化学方程式是_____。
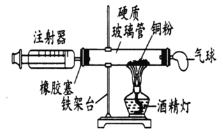
(3)实验室用加热氯化铵和氢氧化钙固体混合物制取氨气,应选择的发生装置是_____。为探究氨气的性质,小红利用图中F装置进行氨气与氧化铜反应的实验,实验中观察到黑色氧化铜粉末变成红色。
(提出问题)得到的红色粉末是什么?
查阅资料:Cu2O是红色,易与稀硫酸反应:Cu2O+H2SO4=CuSO4+Cu+H2O
(猜想假设)红色粉末是①Cu②Cu2O③_____
(设计实验)小明设计如下实验验证红色粉末中是否含有Cu2O:
实验步骤 | 实验现象 | 实验结论 |
取红色粉未于试管中,加人足量稀硫酸 | _____ | 红色粉末中含有Cu2O |
(实验反思)小明设计的实验无法证明红色粉末中是否含有Cu,原因是_____。