题目内容
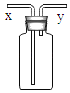
【题目】维生素C泡腾片深受广大消费者喜爱。小林同学查阅了相关资料,了解到泡腾片产生气泡的原因是发生了反应:3NaHCO3+C6H8O7=Na3C6H5O7+3CO2↑+3H2O。他为了测定泡腾片中NaHCO3的质量,进行了如下实验:称量加入水后的饮料瓶及瓶盖中的5片样品的总质量(如图),记录数据为448.50g。将样品加入水中,摇动至无气泡产生,再次称重饮料瓶及瓶盖,记录数据为446.30g。请计算:

(1)生成的CO2的质量为_____。(假设生成的CO2全部逸出)
(2)每片泡腾片中碳酸氢钠的质量。_____(假设泡腾片中的NaHCO3全部参与反应。写出计算过程及结果)
【答案】2.2g 0.84g
【解析】
(1)生成二氧化碳的质量=448.50g-446.30g-2.2g。
(2)设生成2.2g的二氧化碳需要碳酸氢钠的质量为x。

![]() ,x=4.2g
,x=4.2g
故每片泡腾片中含有碳酸氢钠的质量为:4.2g÷5=0.84g。

练习册系列答案
相关题目
【题目】下列实验方法能达到实验目的的是( )
选项 | 实验目的 | 实验方法 |
A | 除去 | 加入足量锌粉 |
B | 检验一瓶气体是否为 | 将燃着的木条伸入瓶中 |
C | 检验蜡烛燃烧的产物中是否有水 | 在火焰上方罩一只冷而干燥的烧杯 |
D | 分离铜粉和铁粉 | 加水,过滤 |
A. A B. B C. C D. D