题目内容
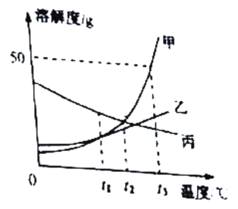
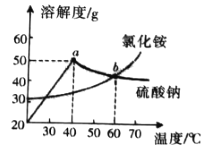
【题目】硫酸钠和氯化铵是重要的化工原料,其溶解度曲线如图所示。下列说法正确的是( )
A.b点表示两者溶液中的溶质质量分数相同
B.40℃时,50g水中恰能溶解50g硫酸钠达到饱和
C.不能用恒温蒸发溶剂的方法从饱和氯化铵溶液中析出晶体
D.将100g硫酸钠饱和溶液从60℃降至40℃,溶液的溶质质量分数不变
【答案】D
【解析】
A、根据曲线,60℃时,氯化铵和硫酸钠的溶解度曲线相交于b点,故b点表示60℃时,两者的溶解度相同,故错误;
B、由图可知,40℃时,硫酸钠的溶解度为50g,故该温度下,100g水中恰能溶解50g硫酸钠达到饱和,故错误;
C、根据曲线,氯化铵的溶解度随温度升高而增大,恒温蒸发溶剂可以从饱和溶液中析出晶体,故错误;
D、将100g硫酸钠饱和溶液从60℃降至40℃,溶解度变大,则没有晶体析出,溶液的溶质质量分数不变,故正确。
故选D

练习册系列答案
相关题目