题目内容
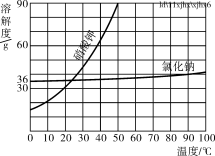
【题目】现有一包含有氯化钠固体的纯碱样品,为测定其成分,同学们取一定质量的这种“纯碱”样品于试管中,加入103g稀盐酸,恰好完全反应,得到4.4g气体.将所得溶液冷却至t℃,恰好成为该温度下的饱和溶液,经测定溶液中的溶质含钠元素的质量为13.8g.求①所加稀盐酸中溶质的质量____;②反应后所得溶液中溶质的质量分数_____.
【答案】7.1% 26.5%
【解析】
设生成4.4g二氧化碳需要碳酸钠质量为x,消耗盐酸为y,生成氯化钠质量为z。
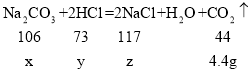
![]() x=10.6g
x=10.6g
![]() y=7.3g
y=7.3g
![]() z=11.7g
z=11.7g
盐酸质量分数=![]() ×100%≈7.1%;
×100%≈7.1%;
根据质量守恒定律,在化学反应中钠元素的质量不变,设溶质质量为m。则有:
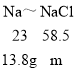
![]() m=35.1g
m=35.1g
原固体中NaCl的质量为:35.1g﹣11.7g=23.4g
所得溶液的质量为:23.4g+10.6g+103g﹣4.4g=132.6g
所得溶液中溶质的质量分数为:![]() 。
。
答:原稀盐酸中的溶质质量分数7.1%,反应后所得的氯化钠溶液的溶质质量分数26.5%。

练习册系列答案
相关题目