题目内容
【题目】早在春秋战国时期,我国就开始生产和使用铁器.
(1)盛水的铁锅与水面接触的一圈最易生锈。钢铁生锈的条件是___________,利用新技术能将不锈钢加工成柔软的金属丝,这是利用了不锈钢的_____(填字母)。
A 耐腐蚀性 B 延展性 C 导热性 D 导电性
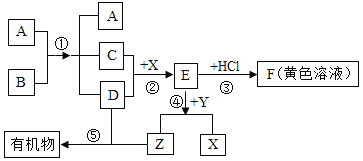
(2)设计从废水中回收硫酸亚铁固体和铜的实验方案如图:
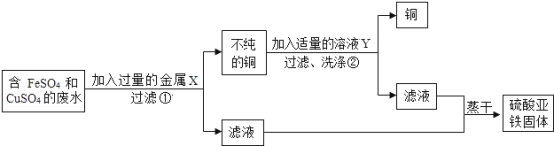
金属X是_____,写出上述实验方案中有关反应的化学方程式①_______②______。
【答案】潮湿空气(或与水、氧气接触) B Fe Fe+CuSO4=Cu+FeSO4 Fe+H2SO4=FeSO4+H2↑
【解析】
(1)盛水的铁锅与水面接触的一圈最易生锈,说明铁生锈的条件是潮湿空气(或与水、氧气接触);可以将不锈钢加工成柔软的金属丝,说明不锈钢具有良好的延展性;
(2)活动性较强的金属可以将位于其后面的金属从它们的盐溶液中置换出来,从含硫酸亚铁和硫酸铜的废水中回收硫酸亚铁固体和铜,可以加入的过量X应是活动性较强的铁,这样即可以得到铜单质,又增加了硫酸亚铁,还不会引入新的杂质;过量的铁可以用Y硫酸使其转化为硫酸亚铁和氢气,有关反应的化学方程式为:Fe+CuSO4=Cu+FeSO4、Fe+H2SO4=FeSO4+H2↑。

 阅读快车系列答案
阅读快车系列答案【题目】某环保小组监测到一湿法冶铜厂排放的废水中含有硫酸和硫酸铜两种污染物,为测定该废水中各污染物的含量,给冶铜厂提供处理废水的参考,环保小组的同学进行了以下实验。取废水200g,向其中加入溶质质量分数为20%的氢氧化钠溶液。测得生成沉淀的质量与所加入的氢氧化钠溶液的质量关系如下表:
加入的氢氧化钠溶液的质量/g | 40 | 80 | 120 | 160 |
生成沉淀的质量/g | 0 | 9.8 | 19.6 | 19.6 |
根据所得数据分析和计算:
(1)向200g该废水中加入足量的氢氧化钠溶液产生沉淀的质量为_____g。
(2)200g该废水中硫酸铜的溶质质量分数_____。
(3)200g该废水中硫酸的溶质质量为_____g。
(4)另取同样的200g该废水,向其中加入17.1%的Ba(OH)2溶液。请你画出加入Ba(OH)2溶液的质量与产生沉淀的质量的关系图。_____(在坐标中作图,并标出曲线折点的坐标)
【题目】化学课上,张老师用排水法收集了一瓶氧气,然后将一根带火星的木条伸入瓶中,结果木条复燃了。
爱动脑筋的小听同学思考:空气中的氧气不能使带火星的木条复燃,而老师收集的氧气却可以,于是提出 了问题:是否只有纯氧才能使带火星的木条复燃呢?张老师告诉同学们:“并不是只有纯氧才能使带火星的 木条复燃”。
(提出问题)究竟气体中氧气的体积分数达到多少才能使带火星的木条复燃?
(探究准备)
(1)兴趣小组的同学先复习了实验室制取氧气的三种方法,最终一致同意选用过氧化氢制取氧气,他们的理由是____(写两条)。
(2)讨论如何获得不同体积分数的氧气。请你帮助他们设计一种收集氧气体积分数为 80%、空气体积分 数为 20%的混合气体的方法:____。
(实验步骤)
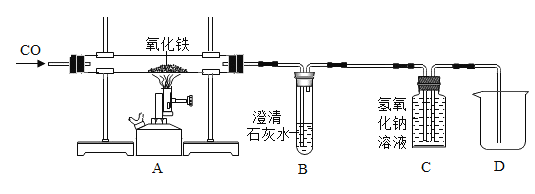
(1)按如图装置组装仪器,检查装置的气密性。
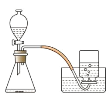
(2)装入药品,分别用 100 毫升的集气瓶收集 5 瓶不同体积分数的氧气。
(3)分别将带火星的木条伸入 5 个集气瓶中,观察实验现象。
(4)记录数据如下表并请你将.表.格.填.写.完.整.。
(记录现象) 实验的数据和现象见下表(已知空气中氧气的体积分数为 21%)。
集气瓶 编号 | 瓶内预装水体积 /mL | 充入氧气体积 /mL | 瓶内空气体积 /mL | 木条能不能 复燃 |
① | 10 | 10 | 90 | 不能 |
② | 20 | 20 | 80 | 不能 |
③ | 30 | ____ | 70 | 不能 |
④ | 40 | 40 | 60 | 能 |
⑤ | 50 | 50 | 50 | ____ |
(讨论与交流)
以上实验刚结束,小听同学脱口而出:氧气的体积分数达到 40%就能使带火星的木条复燃。这个结论遭 到了小语同学的反驳,她反驳的理由是_____。
(反思与总结)
张老师提示,为了使实验结果更加精确,还需要进一步探究,同学们又积极开展探究,部分实验记录如 下表,他们最终得出:混合气体中氧气的体积分数只要达到_____%(保留两位小数)就能使带火星的 木条复燃。
集气瓶 编号 | 瓶内预装水体积 /mL | 充入氧气体积 /mL | 瓶内空气体积 /mL | 木条能不能 复燃 |
… | … | … | … | … |
… | 35 | 35 | 65 | 刚好能 |