题目内容
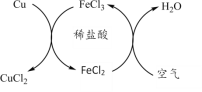
【题目】工业上常采用Cu与稀盐酸在持续通入空气的条件下制取CuCl2。其原理如图所示。下列说法正确的是
A. 反应过程中需不断添加FeCl3溶液
B. 该实验说明Cu能与稀盐酸发生置换反应
C. 通入空气发生的反应为4FeCl2+O2+4HCl=4FeCl3+2H2O
D. 若反应恰好完全进行,将6.4g的铜完全反应,需消耗10.0%的盐酸73.0g
【答案】CD
【解析】
根据原理图示可知,左边的反应(加入铜)反应为Cu+2FeCl3=2FeCl2+CuCl2;右边的反应(通入空气)为4FeCl2+O2+4HCl═4FeCl3+2H2O,总反应相当于为:O2+4HCl+2Cu=2H2O+2CuCl2。
A、由于反应过程中氯化铁是左边反应的反应物,是右边反应的生成物,所以不需要添加FeCl3溶液,故A错误;
B、整个过程反应为O2+4HCl+2Cu=2H2O+2CuCl2,不能说是铜和盐酸发生置换反应,故B错误;
C、根据分析可知,通入空气发生的反应为4FeCl2+O2+4HCl═4FeCl3+2H2O,故C正确;
D、若反应恰好完全进行,将6.4g的铜完全反应,设需消耗10.0%的盐酸的质量为x
![]() x=73g。故D正确。故选CD。
x=73g。故D正确。故选CD。

练习册系列答案
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目