题目内容
【题目】铁及其化合物在生产生活中应用广泛。
(一)铁的性质和应用
(1)图1为某小儿硫酸亚铁糖浆。
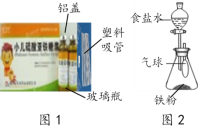
①适当服用该糖浆可治疗______(选填序号)。
A 佝偻病 B 贫血症 C 侏儒症
②图中不涉及到的材料是_______(选填序号)。
A 无机材料 B 合成材料 C 复合材料
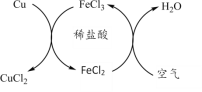
(2)食品保鲜“双吸剂”含铁粉、食盐等,图2为其原理探究实验:
①滴入食盐水后,关闭分液漏斗活塞。一段时间后,铁粉上出现红色固体,气球___(选填“变大”、“不变”或“变小”)。
②食盐水的作用是______。
(二)铁的化合物制备
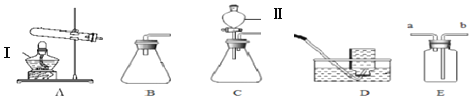
用废铁屑制备铁红(主要成分为Fe2O3)和K2SO4的部分流程如下图所示:
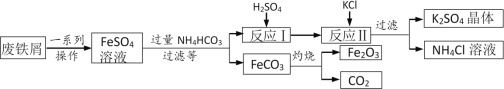
(1)加过量NH4HCO3反应时温度不宜过高的原因为______。
(2)反应Ⅰ生成的气体化学式是______。
(3)K2SO4和NH4Cl在农业生产中都可做______。
(4)为检验K2SO4中是否混有Cl—,要先加入足量_____溶液,静置后再加向上层清液中滴加少量_____溶液。
(5)在空气中灼烧FeCO3的化学方程式为_____。
(三)铁的冶炼和探究
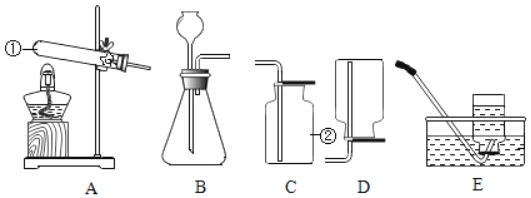
取64.0g Fe2O3粉末,小组同学用下图装置模拟炼铁,并测定反应后固体成分。
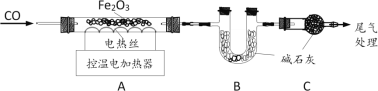
资料:碱石灰可吸收H2O和CO2。
(1)连接装置,先_________,再装入药品。
(2)实验时先通入CO,目的是_____________。
(3)控制A中温度反应,继续通CO至冷却后得到Fe和FeO的黑色固体,装置B中质量增重30.8g。请通过计算回答以下问题:
①固体中FeO质量为_______g。
②A中反应得到该黑色固体的化学方程式为_______。
【答案】B C 变大 加速生锈(或加快铁生锈的反应速率等合理答案均给分) 防止NH4HCO3受热分解 CO2 化肥 Ba(NO3)2 AgNO3 4FeCO3+O2![]() 2Fe2O3+ 4CO2 检查装置气密性 排尽装置内空气,防止爆炸 36.0或36 7CO+4Fe2O3
2Fe2O3+ 4CO2 检查装置气密性 排尽装置内空气,防止爆炸 36.0或36 7CO+4Fe2O3![]() 3Fe+5FeO+7CO2
3Fe+5FeO+7CO2
【解析】
(一)铁的性质和应用:
(1)(a)缺铁性贫血是体内铁的储存不能满足正常红细胞生成的需要而发生的贫血。是由于铁摄入量不足、吸收量减少所至,所以适当服用该糖浆可治疗贫血,故选B ;
(b)铝属于金属材料,塑料属于有机合成材料,玻璃属于无机非金属材料,故选C;
(2)(a)铁粉能与水和氧气反应生成铁锈,滴入食盐水后,关闭分液漏斗活塞。铁粉与水和氧气反应生锈,装置中的压强减小,气球变大;
(b)食盐水的作用是加速生锈(或加快铁生锈的反应速率)等;
(二)铁的化合物制备
(1)碳酸氢铵受热易分解生成氨气、水和二氧化碳。加过量NH4HCO3反应时温度不宜过高的原因为防止NH4HCO3受热分解;
(2)反应Ⅰ是碳酸氢铵与硫酸反应生成硫酸铵、水和二氧化碳,生成的气体化学式是CO2;
(3)K2SO4和NH4Cl存在植物生长所需的钾元素和氮元素,在农业生产中都可做化肥;
(4)Cl-可用硝酸银检验,K2SO4能与硝酸银反应生成硫酸银沉淀和硝酸钾,对Cl-检验产生干扰,Ba(NO3)2 与K2SO4反应生成硫酸钡和硝酸钾,所以先用足量Ba(NO3)2溶液除去K2SO4,排除干扰。为检验K2SO4中是否混有Cl—,要先加入足量Ba(NO3)2溶液,静置后再加向上层清液中滴加少量AgNO3溶液,若生成白色沉淀,则存在Cl-;
(5)根据流程图可知,在空气中灼烧FeCO3的反应是FeCO3和氧气反应生成氧化铁和二氧化碳,化学方程式为4FeCO3+O2![]() 2Fe2O3+ 4CO2;
2Fe2O3+ 4CO2;
(三)铁的冶炼和探究
(1)有气体参加的反应,实验前需要检验装置的气密性,所以连接装置,先检查装置的气密性,再装入药品;
(2)实验时先通入CO,目的是排尽装置内空气,防止爆炸;
(3)装置B中质量的增加30.8g,说明反应过程中有二氧化碳生成,生成二氧化碳的质量为30.8g;根据题意可知,该实验发生的反应是一氧化碳和氧化铁反应生成Fe、FeO和二氧化碳,反应的化学方程式为:7CO+4Fe2O3![]() 3Fe+5FeO+7CO2;
3Fe+5FeO+7CO2;
设:固体中FeO质量为x。

![]() x=36g。
x=36g。

【题目】某化学探究小组以“寻找过氧化氢分解新的催化剂”为课题,开展了下列实验。
(提出问题)氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
(猜想与假设)_____。
(实验探究)
实验步骤 | 实验现象 | 实验结论 |
Ⅰ.分别量取5mL 5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入a g氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 | A试管中产生较多气泡,带火星木条_____,B试管中无明显现象 | ①A试管产生的气体是_____(填化学式)氧化铁可加快过氧化氢的分解速率 |
Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃 | 氧化铁的_____在反应前后均没有发生变化。 |
Ⅲ.将实验II中的剩余物________(填操作名称),并将所得滤渣进行洗涤、干燥、称量 | 所得固体质量仍为a g | 氧化铁的_____在反应前后均没有发生变化。 |
(实验结论)
(1)实验II、III得出结论:_____。
(2)请写出氧化铁催化过氧化氢溶液分解的化学方程式_____。
(实验拓展)
(3)查阅资料得知,CuO、CuSO4、猪肝、马铃薯等也可以做过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是_____。
A MnO2只能作过氧化氢溶液分解的催化剂
B 同一个化学反应可以有多种催化剂
C 催化剂只能加快化学反应的速率
D 用作催化剂的物质不可能是其他反应的反应物或生成物。