题目内容
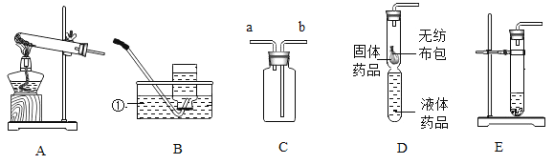
【题目】在老师的指导下,小华和小明利用如图1所示装置对氯酸钾制氧气进行了深入的探究学习。资料:
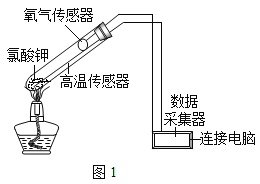
①氯酸钾的熔点约为356℃,二氧化锰的分解温度约为535℃。用酒精灯给物质加热,受热物质的温度一般约为400℃左右;
②不同配比是指氯酸钾和二氧化锰混合物中,氯酸钾和二氧化锰的质量比;
③氯酸钾分解时,传感器得到氧气浓度随温度的变化示意图(图2)及不同配比时氧气浓度随温度的变化示意图(图3)如下:
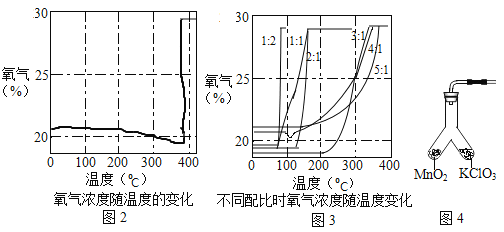
请回答问题:
(1)分析图2,氯酸钾分解温度__________(填“高于”、“等于”或“低于”)其熔点。
(2)分析图2,在氯酸钾分解前,传感器得到氧气浓度降低的可能原因是___________
(3)分析图3,氯酸钾分解温度随物质配比变化的规律是___________,当物质配比为1:2时,氯酸钾分解温度约为________℃。
(4)为证实二氧化锰的催化作用,小华利用如图4装置进行如表所示的实验:
步骤 | 实验操作 | 实验现象 |
Ⅰ | 检查气密性。 | |
Ⅱ | 分别在“Y”形管两侧支管中加入少量二氧化锰和氯酸钾,塞紧橡皮塞。 | |
Ⅲ | 分别用酒精灯先后加热二氧化锰和氯酸钾,用带火星木条放在导管口。 | 加热左侧支管,可观察到_____, 加热右侧支管,可观察到_____。 |
Ⅳ | 冷却后,将“Y”形管左侧支管中部分二氧化锰混入右侧支管中,振荡“Y”形管,加热,用带火星木条放在导管口。 | 加热时间短于步骤Ⅲ,木条很快复燃 |
请回答:
①完善步骤Ⅲ中的填空:加热右侧支管,可观察到________________。
②小华认为根据步骤Ⅳ的实验现象就能说明二氧化锰是氯酸钾分解的催化剂,但小明不同意她的观点,小明认为还需证明在此反应中二氧化锰的__________和__________不变。后来在老师的指导下,小华完善了实验方案,最终验证了自己的结论,则氯酸钾制取氧气的符号表达式___________。
(5)根据氯酸钾的化学式KClO3计算:
①氯酸钾的相对分子质量 ______________
②12.25g氯酸钾中含氧元素 ____________g。
【答案】高于 试管内气压增大,排出一部分空气,使浓度降低 物质配比越大,氯酸钾分解温度越高 70 木条较长时间后复燃 质量 化学性质 KClO3![]() KCl+O2 122.5 4.8
KCl+O2 122.5 4.8
【解析】
(1)通过图中数据可知,氯酸钾的分解温度大约是380℃,氯酸钾的熔点是356℃,所以氯酸钾分解的温度高于其熔点。故答案为:高于;
(2)实验装置内的空气受热膨胀,会发生逸出,导致装置内的氧气浓度降低。所以在氯酸钾分解前,传感器得到氧气浓度降低的可能原因是试管内的压强增大,排出一部分空气。故答案为:试管内气压增大,排出一部分空气,使浓度降低
(3)通过分析图3中的氯酸钾的分解数据可知,氯酸钾分解温度随物质配比变化的规律是配比越大,分解温度越高。当物质配比是1:2时,氯酸钾分解温度约为70℃左右。故答案为:物质配比越大,氯酸钾分解温度越高、70;
(4)Ⅰ、连接装置,将导管放入水中,然后用手紧握Y型管的外壁。观察到导管口有气泡冒出,则证明气密性良好;Ⅱ、没有加热时,氯酸钾不会分解,所以没有任何现象发生;Ⅲ、加热二氧化锰没有氧气生成,所以带火星的小木条不复燃。加热氯酸钾一段时间后,木条复燃;Ⅳ、在二氧化锰的催化作用下,氯酸钾在较低的温度下就能分解生成氧气,操作方法是将Y型管倾斜并抖动,使二氧化锰沿管壁滑入另一侧中。
①加热二氧化锰没有氧气产生,所以木条不复燃;加热氯酸钾一段时间后,木条才复燃。故答案为:木条较长时间后复燃;
②在化学反应中,能改变其他物质的化学反应速率,但是自身的质量和化学性质在化学反应前后不发生改变。这样的物质叫做催化剂。氯酸钾在二氧化锰的催化作用下分解出氯化钾和氧气。故答案为:质量、化学性质、KClO3![]() KCl+O2;
KCl+O2;
(5)①氯酸钾的相对分子质量是一个氯原子的相对原子质量、一个钾原子的相对原子质量、三个氧原子的相对原子质量的加和。即:39×1+35.5×1+16×3=122.5。故答案为:122.5;
②通过①可以计算出,氯酸钾中氧元素的质量分数为:![]() 。则12.25g氯酸钾中,氧元素的质量为:
。则12.25g氯酸钾中,氧元素的质量为:![]() 。故答案为:4.8g。
。故答案为:4.8g。
故答案为(1)高于(2)试管内气压增大,排出一部分空气,使浓度降低(3)物质配比越大,氯酸钾分解温度越高、70(4)①木条较长时间后复燃②质量、化学性质、KClO3![]() KCl+O2(5)①122.5②4.8g
KCl+O2(5)①122.5②4.8g

 阅读快车系列答案
阅读快车系列答案【题目】水是生命之源,也是人类最宝贵的资源。回答下列问题:
(1)节约水资源、防止水污染是每个公民应尽的责任和义务。下列做法正确的是(填序号)___。
A 洗菜后的水用来浇花 B 将大量明矾放入河水中净水
C 合理使用农药化肥,以减少水体污染 D 用水后随手关闭水龙头
(2)向浑浊的水中加入明矾搅拌溶解,此过程中明矾的作用是___;静置一段时间后,进行___(填操作名称),除去固体小颗粒;此操作用到的玻璃仪器除了烧杯、漏斗外还需要___。再向滤液中加入活性炭,利用其___性除去水样中的颜色和异味。
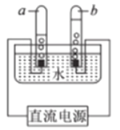
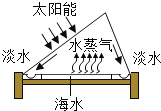
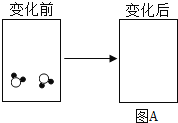
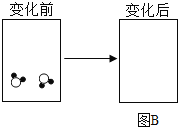
(3)宏观上看,海水淡化和电解水都有物质由液态变成气态的过程,但从微观上看二者有本质的不同。请完成图A和图B,从微观角度画出这种区别。_____
宏观变化 | 微观分析 |
海水淡化示意图 |
|
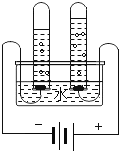
电解水示意图 |
|
(4)电解一定量的水,当与电源正极相连的玻璃管内产生5 mL气体时,理论上与电源负极相连的玻璃管内产生的气体体积是___mL,反应的符号表达式为___。己知同温同压条件下,气体的体积比等于构成气体的分子个数之比,据此计算与电源正极相连的玻璃管内气体和与电源负极相连的玻璃管内气体的质量比为____。