��Ŀ����
����Ŀ��С������һ�ֵ���ɫ�ķ�ĩ��������ɱ����������Ư�ף�������̽���ù���ijɷݡ�
��������⣩�õ���ɫ����Ļ�ѧ�ɷ���ʲô��
���������ϣ�
��1��������һ�ֵ���ɫ���壬������ˮ���ڿ����е�ȼ���ʣ�����һ����ɫ���д̼�����ζ�����塣
��2���������ƣ�Na2O2����һ�ֵ���ɫ���壬����ˮ��Ӧ���������岢�ų��������ȡ�
�����ʵ�鷽����
����һ��ȡ�����ù����ĩ���Թ��У���2mLˮ�����۲�����
����������ȼ�ճ���������ù��壬�ھƾ����ϼ��ȣ��۲�����
�Ƚ�����������������Ϊ����ѷ�����_____����������һ������������������������_____��
��ʵ����֤���ó����ۣ�
С����ʢ�������ù�����Թ��м���2mLˮ�����̹۲쵽����ɫ���ݲ�����������֤���÷�Ӧͬʱ�������������ƣ�NaOH����ȷ���õ���ɫ��ĩΪ�������ƣ�Na2O2����
С����������ɵ�����ɷֽ����жϣ���������������ּ��裺
A ��������CO2 B ��������O2 C ��������H2
��ͬѧ������һ����Ϊ���������е�_____������A������B������C�����϶���������������_____��
��ͨ���������ϣ�ͬѧ���ֵ�֪���ڻ�ѧ��Ӧ�У���Ԫ�ػ��ϼ����ߣ��ͱ�Ȼ��Ԫ�ػ��ϼ۽��͡�����ͨ��С�����ۣ����һ����Ϊ���������е�_____������A������B������C�����϶�Ҳ��������
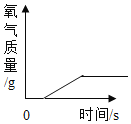
��ͬѧ����ͼ1װ�ã�װ�����������ã�����ʵ����飬��֤�����������ĺ����ԣ�

���ǵķ����ǣ�����ʹˮ�����Թܣ��������ǵ�ľ�����ڵ���_____������a������b������������ľ����ȼ��˵�����ɵ�������������
��С��ͬѧ���Թ��ڹ�����ȫ�ܽ��Ҳ��������ݲ��������Թ��ڼ��������������̣������������������ݣ��ɴ˿�֪����������ˮ��Ӧ�����Һ�к��й������⣬д�����������ڶ������̴��·ֽ�Ļ�ѧ����ʽ��_____��
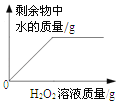
��С��ͬѧ��ͼ2װ�ã�����������������������������������ʱ��������Թܺ���Ͳ�ڵ����嶼��ȴ������ʱ���ܽ��У����Ӧѡ��ͼ2װ���е�_____������A������B������������������_____������ƫ��������ƫС������
�������뷴˼��
���й���Na2O2˵������ȷ����_____������ĸ��ţ���
a��Na2O2����Ԫ�صĻ��ϼ��ǩ�2��
b��Na2O2�����ܷⱣ��
c��Na2O2�Ż�����ˮ����
���������㣩
ͨ����һ���������Ͽ�֪���������� ��Na2O2����ˮ��Ӧʱ���������������ƺ������⣬Ȼ����������ٷֽ�����������ܷ�Ӧ�Ļ�ѧ����ʽΪ��2Na2O2+2H2O��4NaOH+O2����С��ͬѧ��20gij����������Ʒ��������ˮ�У���ַ�Ӧ��������3.2g�����ʲ���ˮ��Ӧ���������Ʒ�й������Ƶ���������_____��
���𰸡�����һ�� ��������Լ��Դ������Ⱦ���� A�� ��Ӧ���в�����̼Ԫ�أ��������ɶ�����̼ a ![]() A�� ƫС b 78%
A�� ƫС b 78%
��������
[���ʵ�鷽��]
���ڿ����е�ȼ��������һ����ɫ���д̼�����ζ���ж��������������Ⱦ���������ϸ��ӣ�������һ�еIJ�����ȡ�����ù����ĩ���Թ��У���2mLˮ�������ˮ����ӦҲ������ˮ���������ƺ�ˮ��Ӧ�������ݣ��ò���������Ⱦ���������ԣ�
�������һ����������Լ��Դ������Ⱦ������
[ʵ����֤���ó�����]
��ͬѧ������һ����Ϊ���������е�A�϶��������������Ƿ�Ӧ���в�����̼Ԫ�أ��������ɶ�����̼��
���A����Ӧ���в�����̼Ԫ�أ��������ɶ�����̼��
��ͨ���������ϣ�ͬѧ���ֵ�֪���ڻ�ѧ��Ӧ�У���Ԫ�ػ��ϼ����ߣ��ͱ�Ȼ��Ԫ�ػ��ϼ۽��͡�����ͨ��С�����ۣ����һ����Ϊ���������е�C�϶�Ҳ������������ڣ�
�����ǵķ����ǣ�����ʹˮ�����Թܣ��Ѵ����ǵ�ľ������a���ܿڴ��������ǵ�ľ����ȼ��˵�����ɵ�������������
���a��
�ܹ������������ڶ������������������·ֽ�����ˮ����������Ӧ�Ļ�ѧ����ʽΪ��![]() ��
��
���![]() ��
��
��Ӧѡ��ͼ2װ���е�A��������A�е�ˮ�ܹ������ȴ������������ƫС��
���A��ƫС��
[�����뷴˼]
a��Na2O2����Ԫ�ػ��ϼ���+1�����ݻ�������Ԫ�ػ��ϼ۴�����Ϊ���֪����Ԫ�صĻ��ϼ��ǩ�1�ۣ���ѡ��˵������ȷ��
b��Na2O2�ܺ�ˮ�Ͷ�����̼��Ӧ�������к���ˮ�����Ͷ�����̼�����ʣ���˱����ܷⱣ�棬��ѡ��˵����ȷ��
c��Na2O2����������ȥ������̼�е�ˮ������������Ϊ�ں�ˮ������һ��ͬʱ��Ҳ�ܺͶ�����̼��Ӧ����ѡ��˵������ȷ��
���b��
�跴Ӧ��������������Ϊx��
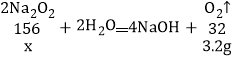
![]()
x��15.6g
�������й������Ƶ���������Ϊ![]() ��
��
�𣺹������й������Ƶ���������Ϊ78%��

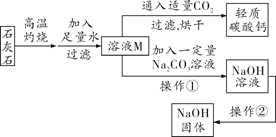
 �¿α�����Ķ�ѵ��ϵ�д�
�¿α�����Ķ�ѵ��ϵ�д�����Ŀ��ѧϰ�˶������̶Թ�������ֽ��д����õ�֪ʶ��ij��ȤС���ͬѧ������⣺�������ܷ��������ڶ������̵Ĵ������أ��������ǽ���������̽����
�����룩
�����������Ƿ�Ӧ�Ĵ�����Ҳ�����뷴Ӧ�������ͻ�ѧ���ʷ�Ӧǰ������䣻
�����������뷴Ӧ������������Ӧǰ���������䣬����ѧ���ʷ����˸ı䣻
���������Ƿ�Ӧ�Ĵ�������Ӧǰ��_____��
��ʵ�飩����ƽ��0.2g�����������Թ�ȡ5mL 5%�Ĺ���������Һ��������ͼʵ�飺

(ע��������������ˮ�����˿���ˮ����)
(1)������
����3���� | ����6��� | ����7���� | ���� |
�����ǵ�ľ����ȼ | _____ | ����������Һ�У�_____ | ����1�������� �������� |
(2)����ٵ�Ŀ����_____��
(3)������ظ�ʵ��ڡ���Ŀ����_____��
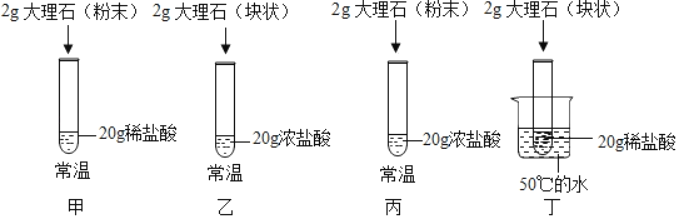
����Ŀ��������ÿ������ʴ�����ϵĽ����豸�Ͳ��ϣ��ߴ������![]() ��ij��ѧС��������������̽����
��ij��ѧС��������������̽����
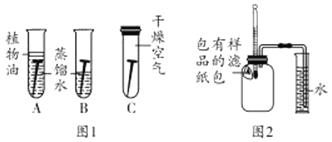
��ʵ��̽����̽��һ��������ʴ��������ͼ1��ʾ��ȡ3����ϸ�����Ⱦ���ͬ������ϸ�����������������뾭���Ѹ����ȴ������ˮ�У�A�Թ��Ϸ���һ��ֲ���ͣ�C�Թ��е��������ڸ���Ŀ����У��Ӹ��ܷ⡣һ��ʱ���۲쵽��A��C��������û�����⣬��B���������⡣����̽���ش��������⡣
![]() �Թ��м�ֲ���͵�����______��
�Թ��м�ֲ���͵�����______��
![]() ������ˮ��е�Ŀ�ģ�______��
������ˮ��е�Ŀ�ģ�______��
![]() ����A��B��C�Թ�����������ʴ������ɴ˿��Եó�����Ʒ��ʴ������______��
����A��B��C�Թ�����������ʴ������ɴ˿��Եó�����Ʒ��ʴ������______��
��ʵ��̽����̽���������۸�ʴ��Ӱ������̽����ͼ2��ʾ����������Ʒ��ʪ����ֽ���ô�ͷ��̶��������ϣ�Ѹ���������۲쵽��Ͳ��ˮ����ϸ�������������ƿ![]() �ݻ�Ϊ
�ݻ�Ϊ![]() �����¶Ȼָ������£�����Ͳ��Һ��߶Ȳ���ʱ����
�����¶Ȼָ������£�����Ͳ��Һ��߶Ȳ���ʱ����![]() ��ʱƿ��������������Ϊ��
��ʱƿ��������������Ϊ��![]() ����¼��ʼ��������Ͳ�Ķ����Լ�����ʱ�������
����¼��ʼ��������Ͳ�Ķ����Լ�����ʱ�������
��� | ���� | ̿�� | NaCl�������� | ��Ͳ��ʼ���� | ��Ͳ���ն��� | ����ʱ�� |
|
|
| 0 | 100 | 60 | Լ190 |
|
|
| 5 | 100 | 60 | Լ140 |
|
|
| 5 | 100 | 60 | Լ160 |
|
|
| 10 | 100 | 60 | Լ175 |
|
|
| 15 | 100 | 60 | Լ185 |
![]() ʵ�鿪ʼ���ƿ���¶�����������˵��������ʴ������______
ʵ�鿪ʼ���ƿ���¶�����������˵��������ʴ������______![]() ��������������������
��������������������![]() ���̡�
���̡�
![]() ʵ�鿪ʼһ��ʱ�����Ͳ�ڵ�ˮ�����ŵ��ܽ��뼯��ƿ�ڣ�ԭ����______��
ʵ�鿪ʼһ��ʱ�����Ͳ�ڵ�ˮ�����ŵ��ܽ��뼯��ƿ�ڣ�ԭ����______��
![]() �����ݱ��Ͽ��Եó�������______
�����ݱ��Ͽ��Եó�������______![]() д��������
�������![]() ��
��
![]() Ӱ�������ʴ�����س����������������Щ��������______�������ʵ��֤������һ������______��
Ӱ�������ʴ�����س����������������Щ��������______�������ʵ��֤������һ������______��