题目内容
【题目】某化学兴趣小组进行空气中氧气含量测定,请你参与实验,并回答下列有关问题:
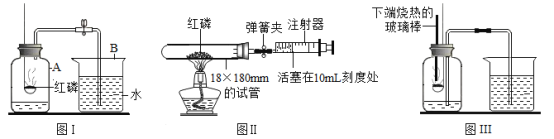
(1)实验过程中,观察到红磷燃烧的现象是 ________;该反应的符号表达式是________ ;上述实验和拉瓦锡研究空气成分实验(将汞与空气封闭在一起加热,生成氧化汞)的化学反应都属于_________ 反应(填基本反应类型).
(2)图Ⅰ实验不仅可以说明氧气占空气的体积分数,还可以说明氮气具有的化学性质有_______(只需写一点).
(3)用图Ⅰ实验装置测定的结果是:集气瓶内水面上升明显大于瓶内空气体积的1/5,你认为导致这一结果的原因是___________ .(只需写一点)
(4)某学生用木炭代替图Ⅰ中的红磷,当木炭停止燃烧,集气瓶冷却到室温.打开弹簧夹后,发现水不能进入集气瓶,原因是_______
(5)图Ⅱ是该兴趣小组的测定空气中氧气含量的改进装置(选用容积为45mL的18×180mm的试管作反应容器),其实验的操作步骤如下:①点燃酒精灯;②撤去酒精灯,待试管冷却后松开弹簧夹;③将少量红磷平装入试管中,将20mL的注射器活塞置于10mL刻度处,并按图Ⅱ中所示的连接方式固定好,再将弹簧夹夹紧橡皮管;④读取注射器活塞的数据.你认为正确的实验操作顺序是 ________________(填序号);图Ⅱ实验中,注射器活塞将从10mL刻度处慢慢前移到约_______ mL处才停止.
(6)经过研究讨论后该兴趣小组又设计了如图Ⅲ的测定空气中氧气含量的改进装置。主要操作是:在实际容积为150mL的集气瓶里,先装进50mL的水,再按图连好仪器,打开止水夹,按下热的玻璃棒,白磷立即被点燃.(已知白磷在空气中燃烧生成五氧化二磷)
①白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是 ________;若实验非常成功,最终集气瓶中水的体积约为___________ mL.
②集气瓶里预先装进的50mL水,在实验过程中起到哪些作用?________ (填写序号)
a 加快集气瓶冷却
b 液封导气管末端以防气体逸出
c 缓冲集气瓶内气压的骤然升高.
【答案】产生白烟,放热 ![]() 化合 不能燃烧 燃烧匙伸入集气瓶时太慢 木炭燃烧消耗氧气是同时生成二氧化碳气体 ③①②④ 1 先降低后升高 70 abc
化合 不能燃烧 燃烧匙伸入集气瓶时太慢 木炭燃烧消耗氧气是同时生成二氧化碳气体 ③①②④ 1 先降低后升高 70 abc
【解析】
(1)实验过程中,观察到红磷燃烧的现象是产生白烟,放热;红磷燃烧生成五氧化二磷,反应的符号表达式为:![]() ;上述实验和拉瓦锡研究空气成分实验(将汞与空气封闭在一起加热,生成氧化汞)的化学反应中,反应物都是两种,生成物都是一种,属于化合反应;
;上述实验和拉瓦锡研究空气成分实验(将汞与空气封闭在一起加热,生成氧化汞)的化学反应中,反应物都是两种,生成物都是一种,属于化合反应;
(2)图Ⅰ实验不仅可以说明氧气占空气的体积分数,还可以说明氮气具有的化学性质有:不能燃烧,不支持燃烧;
(3)用图Ⅰ实验装置测定的结果是:集气瓶内水面上升明显大于瓶内空气体积的五分之一,导致这一结果的原因可能是燃烧匙伸入集气瓶时太慢;
(4)当木炭停止燃烧,集气瓶冷却到室温.打开弹簧夹后,发现水不能进入集气瓶,原因是木炭燃烧消耗氧气是同时生成二氧化碳气体;
(5)正确的实验操作顺序是:将少量红磷平装入试管中,将20mL的注射器活塞置于10mL刻度处,并按图Ⅱ中所示的连接方式固定好,再将弹簧夹夹紧橡皮管,点燃酒精灯,撤去酒精灯,待试管冷却后松开弹簧夹,读取注射器活塞的数据;图Ⅱ实验中,45mL空气中含有氧气的体积约为9mL,注射器活塞将从10mL刻度处慢慢前移到约1 mL处才停止;
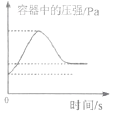
(6)①白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是先降低后升高,这是因为白磷燃烧放热,导致瓶内气压急剧升高,水面下降,完全反应后,温度降低,瓶内气压减小,水面上升;集气瓶中氧气体积约为:100mL×![]() =20mL,若实验非常成功,最终集气瓶中水的体积约为:50mL+20mL=70mL;
=20mL,若实验非常成功,最终集气瓶中水的体积约为:50mL+20mL=70mL;
②集气瓶里预先装进的50mL水,在实验过程中能够加快集气瓶冷却,液封导气管末端以防气体逸出,缓冲集气瓶内气压的骤然升高。