题目内容
【题目】水是宝贵的自然资源,日常生活、工农业生产和科学实验都离不开水。
(1)如图为自来水厂净化过程示意图。
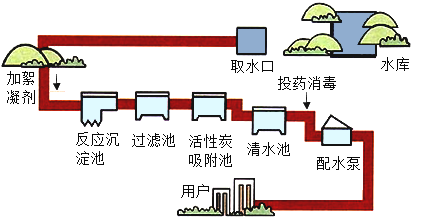
①下列有关水的净化的说法不正确的是_____。
A过滤能使硬水转化为软水
B净水时活性炭能起吸附作用
C自来水厂净水过程包括蒸馏
D电解水是一种常用的净水方法
②硫酸铝可作絮凝剂。写出用铝和稀硫酸制硫酸铝的化学方程式_____。
③高铁酸钾(K2FeO4)是一种新型高效水处理消毒剂,其生产过程的两个主要反应如下:3NaClO+4NaOH+2Fe(OH)3=2Na2FeO4+3NaCl+5_____;Na2FeO4+2KOH=K2FeO4↓+2NaOH,该反应所属基本反应类型为_____。
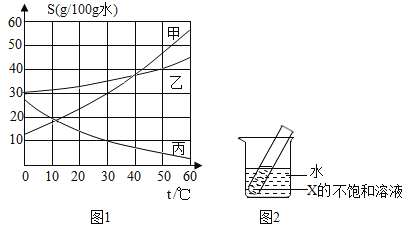
(2)如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线,请分析回答:
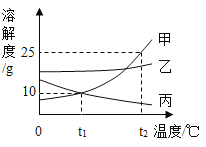
①t1℃时,甲的溶解度_____(填“>”或“<”或“=”)丙的溶解度。
②t2℃时,将50g甲放入100g水中,充分搅拌后,所得溶液的溶质质量分数为_____,该溶液为_____(填“饱和”或“不饱和”)溶液。
③0℃时,分别将甲、乙、丙三种物质的饱和溶液各100g升温到t2℃时,所得溶液的溶质质量分数由大到小的顺序是_____。
【答案】ACD ![]() H2O 复分解反应 = 20% 饱和 乙>甲>丙(或乙甲丙)
H2O 复分解反应 = 20% 饱和 乙>甲>丙(或乙甲丙)
【解析】
(1)①A、过滤只能除去水中的不溶性杂质,不能除去水中的可溶性钙、镁化合物,不能将硬水软化,符合题意;
B、活性炭具有吸附性,可以吸附水中的色素和异味,不符合题意;
C、自来水厂净水过程包括沉降、过滤、吸附、消毒,不包括蒸馏,符合题意;
D、电解水不属于净水方法,符合题意。
故选ACD;
②铝能与稀硫酸反应生成硫酸铝和氢气,该反应的化学方程式为:![]() ;
;
③根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含7个钠原子、3个氯原子、13个氧原子、10个氢原子、2个铁原子,生成物中含7个钠原子、2个铁原子、8个氧原子、3个氯原子,故还应含10个氢原子,5个氧原子,故将化学方程式补充完整为:![]() ;
;
![]() ,根据化学方程式,该反应符合“两种化合物互相交换成分生成另外两种化合物”的反应,属于复分解反应;
,根据化学方程式,该反应符合“两种化合物互相交换成分生成另外两种化合物”的反应,属于复分解反应;
(2)①由图可知,t1℃时,甲的溶解度曲线与乙的溶解度曲线相交,故该温度下,甲的溶解度=乙的溶解度;
②由图可知,t2℃时,甲的溶解度为25g,即该温度下,100g溶剂中最多能溶解25g甲物质,将50g甲放入100g水中,充分搅拌后,所得溶液为饱和溶液,故该溶液的溶质质量分数为:![]() ,故填:20%,饱和;
,故填:20%,饱和;
③由图可知,甲、乙的溶解度随温度的升高而增加,丙的溶解度随温度的升高而减小,故0℃时,分别将甲、乙、丙三种物质的饱和溶液各100g升温到t2℃时,甲、乙变为不饱和溶液,升温后,溶质质量分数不变,丙还是饱和溶液,0℃时,乙的溶解度大于甲的溶解度大于t2℃时,丙的溶解度,故0℃时,乙的饱和溶液的溶质质量分数大于甲的饱和溶液的溶质质量分数大于t2℃时丙的饱和溶液的溶质质量分数,故0℃时,分别将甲、乙、丙三种物质的饱和溶液各100g升温到t2℃时,所得溶液的溶质质量分数由大到小的顺序是:乙>甲>丙。

 阅读快车系列答案
阅读快车系列答案【题目】某小组在学习“二氧化碳与氢氧化钠溶液反应”时,进行了如下探究
(提出问题)二氧化碳是与氢氧化钠反应,还是微溶于水中?
(查阅资料)①15℃时,101KPa时,二氧化碳的溶解度如表;
溶剂 | 水 | 酒精 |
溶解度 | 1.0 | 0.3 |
②15℃时,在酒精中,氢氧化钠易溶,碳酸钠微溶.
③通常情况下,稀溶液的体积约等于溶剂的体积.
(实验设计)在15℃、101KPa时,制取二氧化碳并用于实验

(分析与表达)
(1)如果二氧化碳与氢氧化钠反应,化学方程式是__,那么氢氧化钠应__保存.
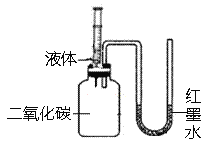
(2)实验前,两套装置都进行了气密性检查.实验乙装置气密性检查的方法是__.
(3)实验甲中,同时滴入等体积的水和氢氧化钠溶液后的现象是__.
(4)实验乙中,将氢氧化钠溶液完全滴入锥形瓶中,注射器活塞会自动向内移动并将酒精推入锥形瓶中,还可能观察到的现象是__.
(5)实验乙结束后,注射器中酒精体积为20mL,则锥形瓶和胶头滴管中剩余的二氧化碳体积为__mL,与氢氧化钠反应的二氧化碳体积为__mL.
【题目】某品牌饼干的配料为:小麦粉、食用油、食用盐、碳酸钙、食品添加剂(碳酸氢钠)等。饼干制作的烘焙过程中,碳酸氢钠受热全部分解转化为碳酸钠,而碳酸钠、碳酸钙不分解。已知:碱石灰中含氧化钙、氢氧化钠等。某校研究性学习小组对其成分进行了如下探究。
Ⅰ、定性判断饼干中有关成分。
取一小包饼干。研碎后放入烧杯,加入适量蒸馏水,用玻璃棒搅拌,得到待检液。
实验操作和现象 | 实验结论 | |
碳酸盐的检验 | 在试管中加入少量待检液和足量稀盐酸,有气泡产生;将产生的气体通入澄清石灰水,澄清石灰水变浑浊 | 饼干中含有_____(填离子符号) |
(交流讨论)
饼干中的碳酸钙与稀盐酸反应的化学方程式为_____。
(深入探究)如何进一步确认饼干中含有两种碳酸盐?
将剩余待检液过滤,用蒸馏水洗涤固体2至3次;将_____与稀盐酸反应,根据反应的现象,则证明饼干中既有碳酸钙,又有碳酸钠。
Ⅱ、定量检测:一小包饼干中碳酸钠质量的测定。
(实验装置)
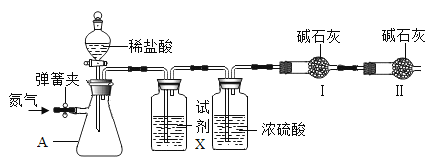
(实验步骤)
①按如图连接好装置,检查气密性;
②取一小包饼干研碎后放入烧杯,加入适量蒸馏水、用玻璃棒充分搅拌后,过滤,洗涤;
③将滤液和洗涤液合并后倒入容器A,按图示装入其他药品(试剂X用于吸收挥发出来的HCl,它不与CO2反应);
④打开弹簧夹,向装置中通入一段时间N2后,关闭弹簧夹;
⑤用电子天平称量干燥管Ⅰ的质量,记录数据m1;
⑥逐滴加入稀盐酸至不再产生气泡时,停止滴加;
⑦_____;
⑧重复步骤⑤,记录数据m2。
(交流讨论)(1)步骤③将滤液和洗涤液合并的原因是_____。
(2)试剂X可以是下列物质中的_____(填字母)。
ANaHCO3溶液 BNaOH溶液 CAgNO3溶液
(3)装置Ⅱ的作用是_____。
(数据处理)m2﹣m1=0.088g,则这包饼干中碳酸钠的质量为_____g。