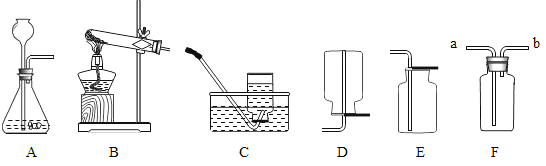
题目内容
【题目】碳酸钠和碳酸氢钠是生活中常见的盐,通过实验验证、探究它们的化学性质.
(查阅资料)
①Na2CO3+CaCl2═CaCO3↓+2NaCl
②2NaHCO3![]() Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
③Ca(HCO3)2 易溶于水.
④CaCl2 溶液分别与 NaHCO3、Na2CO3 溶液等体积混合现象(表中的百分数为溶液中溶质的质量分数):
NaHCO3 | Na2CO3 | ||||
0.1% | 1% | 5% | 0.1% | ||
CaCl2 | 0.1% | 无明显现象 | 有浑浊 | 有浑浊 | 有浑浊 |
1% | 无明显现象 | 有浑浊 | 有浑浊,有微小气泡 | 有沉淀 | |
5% | 无明显现象 | 有浑浊 | 有沉淀,有大量气泡 | 有沉淀 | |
(进行实验)
序号 | 实验装置 | 主要实验步骤 | 实验现象 |
实验 1 |
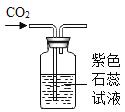
| 向2支试管中分别加入少 量Na2CO3 和 NaHCO3 溶液,再分别滴加盐酸 | 2 |
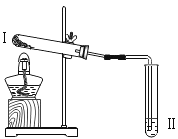
实验 2 |
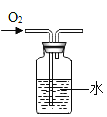
| 向Ⅱ中加入试剂a,向Ⅰ中 加入少量Na2CO3或 NaHCO3 固体,分别加热一段时间 | Na2CO3 受热时Ⅱ中无明 显现象 NaHCO3 受热时Ⅱ中出现浑浊 |
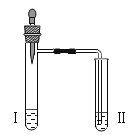
实验 3 |
| 向Ⅱ中加入试剂 a,向Ⅰ中 加入少量 5%的 NaHCO3 溶 液,再滴加 5%的 CaCl2 溶 液 | Ⅰ中出现浑浊,有气泡产 生Ⅱ中出现浑浊 |
(解释与结论)
(1)实验1中,NaHCO3与盐酸反应的化学方程式为_____.
(2)实验2中,试剂a为_____.
(3)实验3中,NaHCO3 与 CaCl2 反应的化学方程式为:2NaHCO3+CaCl2═_____+_____+_____+H2O
(反思与评价)
(1)实验 2 中,加热 NaHCO3后,试管Ⅰ中残留固体成分可能为_____(写出所有可能).
(2)资料④中,NaHCO3溶液与 CaCl2 溶液混合的现象中,有些只观察到浑浊、未观察到气泡,原因可能是_____.
(3)用2种不同的方法鉴别Na2CO3和NaHCO3 固体,实验方案分别为:
①_____.
②_____.
【答案】![]() 澄清的石灰水 CaCO3↓ 2NaCl CO2↑ Na2CO3; Na2CO3,NaHCO3 CaCl2溶液的溶质质量分数较小,生成的 CO2 量较少,CO2溶于水,因此没有气泡 各取少量 0.1% 的 NaHCO3 和 Na2CO3 加入等质量的 5%的 CaCl2 溶液,若无明显现象,则为 NaHCO3,若观察到浑浊则为 Na2CO3 各取少量 Na2CO3 和 NaHCO3固体于实验 2 装置中,若观察到澄清石灰水变浑浊,固体为 NaHCO3,若观察到无明显现象,固体为 Na2CO3
澄清的石灰水 CaCO3↓ 2NaCl CO2↑ Na2CO3; Na2CO3,NaHCO3 CaCl2溶液的溶质质量分数较小,生成的 CO2 量较少,CO2溶于水,因此没有气泡 各取少量 0.1% 的 NaHCO3 和 Na2CO3 加入等质量的 5%的 CaCl2 溶液,若无明显现象,则为 NaHCO3,若观察到浑浊则为 Na2CO3 各取少量 Na2CO3 和 NaHCO3固体于实验 2 装置中,若观察到澄清石灰水变浑浊,固体为 NaHCO3,若观察到无明显现象,固体为 Na2CO3
【解析】
[解释与结论]
(1)用质量守恒定律写碳酸氢钠和盐酸反应的化学方程式;
(2)从装置可看出是检验碳酸氢钠和碳酸钠的热稳定性,再结合二氧化碳能使澄清的石灰水变浑浊,分析解答;
(3)用质量守恒定律写NaHCO3 与 CaCl2 反应的化学方程式;
[反思与评价]
(1)根据NaHCO3是否完全分解解答;
(2)根据CaCl2溶液的溶质质量分数较小,生成的 CO2 量较少,CO2溶于水解答;
(3)根据Na2CO3和NaHCO3 固体的性质解答。
[解释与结论]
(1)碳酸氢钠和盐酸反应生成水和二氧化碳,故答案:NaHCO3+HCl═NaCl+H2O+CO2↑.
(2)本实验是为检验碳酸钠和碳酸氢钠的热稳定性.故实验中的实验步骤是加热并将产生的气体通入澄清的石灰水中;
(3)NaHCO3 与 CaCl2 反应的化学方程式2NaHCO3+CaCl2=CaCO3↓+2NaCl+CO2↑+H2O
[反思与评价]
(1)NaHCO3完全分解时,试管Ⅰ中残留固体成分为Na2CO3,没有完全分解时Na2CO3,NaHCO3;
(2)NaHCO3溶液与 CaCl2 溶液混合的现象中,有些只观察到浑浊、未观察到气泡,原因可能是CaCl2溶液的溶质质量分数较小,生成的 CO2 量较少,CO2溶于水,因此没有气泡;
(3)①各取少量 0.1% 的 NaHCO3 和 Na2CO3 加入等质量的 5%的 CaCl2 溶液,若无明显现象,则为 NaHCO3,若观察到浑浊则为 Na2CO3
②各取少量 Na2CO3 和 NaHCO3固体于实验 2 装置中,若观察到澄清石灰水变浑浊,固体为 NaHCO3,若观察到无明显现象,固体为 Na2CO3
故答案:
[解释与结论]
(1)![]() (2)澄清的石灰水(3)CaCO3↓ 2NaCl CO2↑
(2)澄清的石灰水(3)CaCO3↓ 2NaCl CO2↑
[反思与评价]
(1)Na2CO3 ;Na2CO3,NaHCO3;(2)CaCl2溶液的溶质质量分数较小,生成的 CO2 量较少,CO2溶于水,因此没有气泡(3)①各取少量 0.1% 的 NaHCO3 和 Na2CO3 加入等质量的 5%的 CaCl2 溶液,若无明显现象,则为 NaHCO3,若观察到浑浊则为 Na2CO3②各取少量 Na2CO3 和 NaHCO3固体于实验 2 装置中,若观察到澄清石灰水变浑浊,固体为 NaHCO3,若观察到无明显现象,固体为 Na2CO3

【题目】下表是![]() 和
和![]() 在不同温度时的溶解度,回答问题。
在不同温度时的溶解度,回答问题。
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g |
| 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | |
I.两种物质中,溶解度受温度影响变化较大的是_____。
II.除去![]() 中少量的
中少量的![]() ,步骤是:加水溶解,蒸发浓缩,_____,过滤,洗涤,干燥。
,步骤是:加水溶解,蒸发浓缩,_____,过滤,洗涤,干燥。
III.50℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到50℃,剩余溶液的质量:![]() 溶液_____(填“大于”、“等于”或“小于”)
溶液_____(填“大于”、“等于”或“小于”)![]() 溶液。
溶液。
IV.![]()

A中溶液_____(填“饱和”或“不饱和”)溶液,C中溶液的总质量是_____g。
【题目】五水硫酸铜(化学式:CuSO4·5H2O)也被称作硫酸铜晶体,在电镀、印染、颜料、农药、医药等方面有广泛应用。
(1)游泳池中的水常显蓝色,是因为向其中洒入了一些硫酸铜晶体,其目的是_____。
(2)农药波尔多液的化学制备原理是硫酸铜与熟石灰发生反应,生成的碱式硫酸铜,具有很强的杀菌能力。Ca(OH)+2CuSO=X+Cu(OH)SO4↓,请写出X的化学式_____。
(3)依据下表中硫酸铜的溶解度数据,若要从溶液中得到硫酸铜晶体较好的方法是_____。
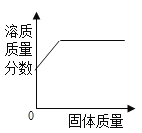
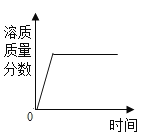
(4)硫酸铜晶体在加热时会逐步失去结晶水直至完全失去结晶水变成白色无水物。请根据所给图像,写出从45℃到110℃发生反应的化学方程式_____。
硫酸铜在不同温度下的溶解度
温度 | 0 | 10 | 20 | 30 | 40 | 50 |
溶解度S/g | 14.3 | 17.4 | 20.7 | 25.0 | 28.5 | 33.3 |
温度℃ | 60 | 70 | 80 | 90 | 100 | |
溶解度S/g | 40.0 | 47.1 | 55 | 64.2 | 75.4 |

(5)由黄铜矿(CuFeS2)制取硫酸铜晶体有以下两种方法:
传统法:①焙烧 ②稀硫酸酸浸 ③除杂 ④结晶 ⑤甩干
改进法:①浓硫酸酸浸 ②水溶 ③除杂 ④结晶 ⑤甩干
(问题1)两种工艺中除杂时都要适当调高pH值以更好地除去其中的铁元素,下列加入的物质能达到此目的的是_____。
A Cu B CuO C NaOH D Cu(OH)2
(问题2)水溶时,加入的水量不宜太多。一是为了考虑节约原料,二是为了_____。
(问题3)除杂后过滤出滤液时,要趁热过滤的原因是_____。
(问题4)最后一步干燥时,选择甩干而不选择常用的烘干,理由是_____
(问题5)改进法与传统法相比,你认为最大的优点是_____。