题目内容
【题目】高锰酸钾在生产、生活中有广泛应用。实验小组对高锰酸钾的腐蚀性进行研究。
(进行实验)
实验1:将新鲜鸡皮在不同浓度的KMnO4溶液中浸泡相同时间,现象如下表。
KMnO4溶液浓度 | 0.002% | 0.01% | 0.1% | 1% |
鸡皮的变化 | 无明显变化 | 边缘部分变为棕黄色 | 全部变为棕色 | 全部变为黑色 |
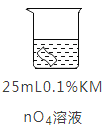
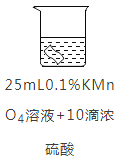
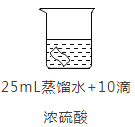
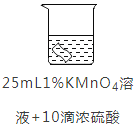
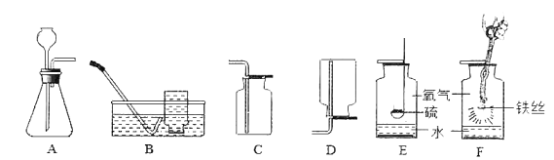
实验2:将铜片分别浸泡在4种溶液中进行实验,所得数据如下表。
编号 | ① | ② | ③ | ④ | |
实验 |
|
|
|
| |
铜片质量/g | 实验前 | 0.54 | 0.54 | 0.54 | 0.54 |
18小时后 | 0. 54 | 0. 52 | 0. 54 | 0. 43 | |
(解释与结论)
(
(2)实验2中,设计实验③的目的是__________。
(3)实验2中,通过对比②和④,得出的结论是__________。
(4)实验2中,欲得出“KMnO4和硫酸共同作用对铜才有腐蚀性”的结论,需要对比_________ (填编号)。
(5)实验2中,铜片被腐蚀的反应如下,补全该反应的化学方程式。5Cu + 2KMnO4+ 8H2SO4=5CuSO4 + 2MnSO4 + K2SO4+_________
【答案】其他条件相同时,高锰酸钾溶液浓度越大对鸡皮的腐蚀性越强 空白对照实验,验证只有浓硫酸不能腐蚀铜片 其他条件相同时,酸性高锰酸钾溶液浓度大对铜的腐蚀性强 ①②③ 8H2O
【解析】
(1)实验1的结论是其他条件相同时,高锰酸钾溶液浓度越大对鸡皮的腐蚀性越强;
(2)实验2中,设计实验③的目的是空白对照实验,验证只有浓硫酸不能腐蚀铜片;
(3)实验2中,通过对比②和④,得出的结论是其他条件相同时,酸性高锰酸钾溶液浓度大对铜的腐蚀性强;
(4)实验2中,欲得出“KMnO4和硫酸共同作用对铜才有腐蚀性”的结论,需要对比①②③,通过对比①②可知,高锰酸钾在酸性条件下才具有腐蚀性,通过对比②③可知,只有酸性溶液不具有腐蚀性,通过对比①②③可知,KMnO4和硫酸共同作用对铜才有腐蚀性;
(5)由化学方程式5Cu + 2KMnO4+ 8H2SO4=5CuSO4 + 2MnSO4 + K2SO4+_________可知,反应物中有5个铜原子,2个钟原子2个锰原子,40个氧原子,16个氢原子,8个硫原子,生成物中有5个铜原子,8个硫原子,32个氧原子,2个锰原子,2个钾原子,根据质量守恒定律,在化学变化中,原子的种类和数目不变,所以得出空白处为:8H2O。

【题目】化学兴趣小组在实验室用氯酸钾和二氧化锰混合加热制取氧气,该反应的化学表达式为________。某次实验时偶然发现制得的气体有刺激性气味,这一现象引起了同学们的兴趣,于是在老师的指导下对该气体成分进行探究。
【提出问题】氯酸钾与二氧化锰混合加热后产生的气体成分是什么?
【查阅资料】
①氯酸钾与二氧化锰混合加热产生的气体只以单质形式存在;
②氯气(Cl2)是有刺激性气味的气体,能溶于水,能使湿润的淀粉碘化钾试纸变蓝。
【猜想假设】
猜想一:该气体为O2;猜想二:该气体为______;猜想三:该气体为O2和Cl2的混合物。
【实验探究】
序号 | 操作 | 现象 | 结论 |
方案Ⅰ | 用排水集气法收集甲、乙两瓶气体,将带火星的木条伸入甲瓶,湿润的淀粉碘化钾试纸伸入乙瓶。 | 木条复燃, 淀粉碘化钾试纸不变色 | 猜想_______成立 |
方案Ⅱ | 向上排空气法收集甲、乙两瓶气体,将带火星的木条伸入甲瓶,湿润的淀粉碘化钾试纸伸入乙瓶。 | 木条______, 淀粉碘化钾试纸为___色 | 猜想三成立 |
【反思评价】
为什么两种方案得出的结论不一致?哪个是正确的?
①同学:方案Ⅰ结论不正确,其操作不合理,不合理之处是__________。
②老师:不需要进行实验,就能排除猜想一,理由是__________。
【拓展应用】
实验结束后,该组同学准备回收固体剩余物中的不溶物二氧化锰,实验的主要步骤为:①溶解、②________、③洗涤干燥。步骤②中玻璃棒的作用是_________。