题目内容
【题目】下面是部分原子或离子的结构示意图.请仔细观察、分析,再回答问题:
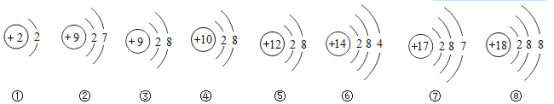
(1)上述粒子中属于阳离子的是_________________;(填序号),属于阴离子的是___________(填序号)。
(2)上述粒子中属于稳定结构的原子是_________________;(填序号).可见,元素的化学性质与原子的________________关系密切。
(3)写出⑤和⑦形成化合物的化学式______________。
【答案】⑤ ③ ①④⑧ 最外层电子数 MgCl2
【解析】
(1)原子失去电子变为阳离子,表现的特征为核外电子数小于核电荷数,因此属于阳离子的是:⑤;则属于阴离子的是③;
(2)最外层电子数为8(或2)时,达到稳定结构,属于稳定结构的是:①、③、④、⑤、⑧,但其中属于原子的是①④⑧;元素的化学性质与其原子的最外层电子数有关;
(3)⑤核电荷数为12,因此为Mg,⑦核电荷数为17,为Cl,因此形成的化合物化学式为:MgCl2。

 名校课堂系列答案
名校课堂系列答案【题目】小滨同学为了测定某珍珠粉中钙元素的质量分数,称取12.5g珍珠粉样品,进行四次高温煅烧、冷却、称量剩余固体的重复操作(杂质不参加反应),记录数据如下:
操作次序 | 第一次 | 第二次 | 第三次 | 第四次 |
剩余固体质量/g | 10.8 | 9.6 | 8.1 | 8.1 |
(1)完全反应后生成二氧化碳的质量为________________________ g。
(2)求该珍珠粉中碳酸钙的质量分数___________________。
(3)求该珍珠粉中钙元素的质量分数___________________。
【题目】为测定某黄铜(铜锌合金)样品中铜的含量,某化学活动小组分三次进行实验,实验数据如表,请回答下列问题:
所取药品 | 第一次 | 第二次 | 第三次 |
黄铜样品质量 | 12g | 10g | 10g |
烧杯+稀盐酸质量 | 150g | 150g | 160g |
充分反应后,烧杯+剩余物质质量 | 161.8g | 159.8g | 169.8g |
(1)第_______次实验中,稀盐酸和样品恰好完全反应。
(2)黄铜样品中铜的质量分数是多少_______?(写出计算过程)
(3)第三次实验充分反应后所得溶液中的溶质为________________(写化学式)
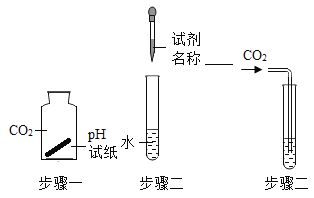
【题目】甲、乙二个实验用于验证水的性质。
甲:验证水与二氧化碳反应 | 乙:验证水与生石灰反应 |
|
|
①写出甲实验化学反应方程式_________。步骤二,胶头滴管中试剂名称是________。
②乙实验发生反应时出现现象是________。
③甲、乙实验都使用酸碱指示剂,其目的是______________。