题目内容
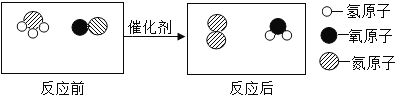
【题目】一氧化氮是一种大气污染物,利用它与液氨的反应可减少其排放。结合微观示意图分析,下列结论正确的是( )
A. 反应前后各元素的化合价均不变
B. 反应中涉及到的含氮化合物有3种
C. 发生反应的液氨和一氧化氮的分子个数比为2:3
D. 参加反应的液氨与生成水的质量比为17:18
【答案】C
【解析】
A、观察微观示意图中的反应物的分子为:NH3和NO,生成物的分子为N2和H2O,根据质量守恒定律,反应的方程式为:4NH3+6NO 5N2+6H2O。反应前氮元素由化合物变成单质,即由-3、+2变成0,化合价发生了改变,故说法错误;
5N2+6H2O。反应前氮元素由化合物变成单质,即由-3、+2变成0,化合价发生了改变,故说法错误;
B、反应物中含氮元素的化合物分别是NH3和NO两种,故说法错误;
C、根据方程式可知,发生反应的液氨和一氧化氮的分子个数比为4:6=2:3,故说法正确;
D、根据方程式参加反应的液氨与生成水的质量比为[4×(14+3)]:[6×(2+16)]=17:27,故说法错误。
故选:C。

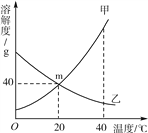
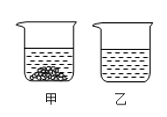
【题目】氯化钠(NaCl) 和硝酸钾 (KNO3) 在不同温度时的溶解度如下表,20℃时甲乙两个烧杯中各有100g水,分别都加入质量为m的氯化钠和硝酸钾固体,充分溶解后如图所示:
温度(℃) | 10 | 20 | 40 | 60 | 80 | |
溶解 度/g | KNO3 | 20.9 | 31.6 | 63.9 | 110 | 169 |
NaCl | 35.8 | 36 | 36.6 | 37.3 | 38.4 | |
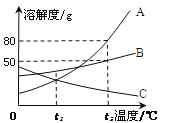
(1)氯化钠和硝酸钾两种物质中,溶解度受温度影响较大的是_____________。
(2)甲中溶解的物质是__________。
(3)常温下配制100g氯化钠的饱和溶液,所需的玻璃仪器有___________。
(4)下列说法正确的是___________
A 若将甲、乙烧杯中的溶液都升温到40℃,所得溶液均不饱和
B 若将甲、乙烧杯中的溶液都降温到10℃,可能都会有固体析出
C 若向甲中加入20g水,则甲中的溶液一定变为不饱和
D 硝酸钾中混有少量的氯化钠,可采用蒸发结晶的方法提纯硝酸钾
【题目】分类类比是初中化学常用的学习方法。
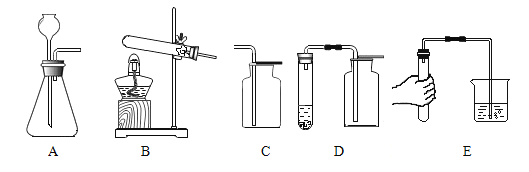
(1)初中化学有许多实验,若按照实验目的不同,找出一个与众不同的实验___(填字母);选择的依据是___。
|
|
|
|
A 将红热的木炭伸入盛有氧气的集气瓶中 | B 将燃着的硫伸入盛有氧气的集气瓶中 | C 将打磨过的铝丝浸入硫酸铜溶液中 | D 在蓝色火焰上方罩一个冷而干的烧杯 |
(2)二氧化硫和二氧化碳的化学性质相似,能与水反应生成亚硫酸,请写出将二氧化硫气体通入到氨水中反应的化学方程式___;亚硫酸和碳酸的化学性质相似,如常温下易分解,亚硫酸钠也能与硫酸发生反应,请写出此反应的化学方程式___。
【题目】学习化学知识和技能,可以帮助我们鉴别和检验物质。
(1)在实验室鉴别白酒与白醋,可采用的方法是____。
(2)现有两瓶失去标签的无色溶液,其中一瓶是氢氧化钙溶液,一瓶是稀盐酸。为了鉴别它们,同学们设计了如下实验方案:先给两瓶溶液贴上标签A、B,然后分别取样进行实验。请将横线部分填写完整:
加入的试剂 | 现象 | 结论 | |
方案1 | 二氧化碳 | A中出现白色浑浊,B中无明显现象。 | A是____溶液, B是另一种溶液。 |
方案2 | 碳酸钠溶液 | _____。 | |
方案3 | 试剂X | …… |
写出方案1中发生反应的化学方程式____。
(方法感悟)在鉴别物质时,要先分析物质的性质,然后选择恰当的试剂,必须产生不同现象才能达到鉴别物质的目的。
(拓展应用)完成方案3,请从下列提供的试剂中选出所有能鉴别出这两种物质的试剂X ____。(填序号)
①酚酞溶液 ②pH试纸 ③镁 ④氧化铜 ⑤稀硝酸 ⑥氢氧化铜 ⑦氯化镁溶液 ⑧硝酸钡溶液
(3)小华同学对方案2进一步探究,设计了如下实验方案:
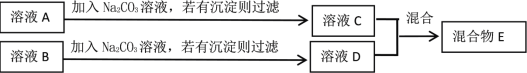
溶液C和溶液D混合,可能会出现以下三种情况:
①有沉淀产生时,写出其中发生反应的化学方程式____。
②有气泡冒出时,可通过现象反推出溶液C中的溶质是____。
③无明显现象时,混合物E中一定含有的溶质的化学式____。