题目内容
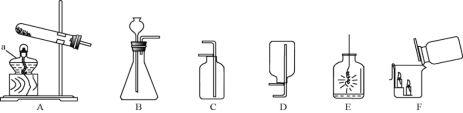
【题目】探究题。化学兴趣小组的同学用如图所示装置进行中和反应实验,请你参与下列探究:
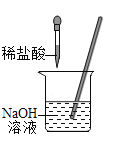
(1)为确定稀盐酸与氢氧化钠溶液是否刚好完全中和,小华取出一定量反应后的溶液于一支试管中,向其中滴入几滴无色酚酞试液,振荡,观察到酚酞试液不变色,于是他得出“两种物质已恰好完全中和”的结论。
①写出该中和反应的化学方程式:___________________。
②小亮认为小华得出的结论不完整,他认为除了“恰好中和”外,还有第二种可能性,这种可能性是__________________。
③请你另外设计一个实验,探究上述烧杯中的溶液是否恰好完全中和,填写下表(选择甲、乙中的一个作答):
实验 | 实验方法 | 实验现象 | 实验结论 |
甲 | _______ | _______ | 恰好中和 |
乙 | ______ | _________ | 第二种可能性 |
(2)玲玲同学在实验时,发现烧杯中有少量的气泡产生,她经过分析认为可能的原因是氢氧化钠溶液变质(提示:碳酸钠溶液呈碱性)。为了检验氢氧化钠溶液是否变质,玲玲提出用酚酞试液检验,你认为该方法________(填“正确”或“不正确”),理由是_____________。
(3)中和反应在实际生产、生活中应用极为广泛,请你举一具体实例加以说明:____________。
【答案】![]() 稀盐酸过量 取反应后溶液适量于试管中,滴加石蕊试液 石蕊试液不变色 取反应后溶液适量于试管中,滴加石蕊试液 石蕊试液变红色 不正确 氢氧化钠、碳酸钠溶液显碱性,都能使酚酞试液变红色 利用熟石灰改良酸性土壤
稀盐酸过量 取反应后溶液适量于试管中,滴加石蕊试液 石蕊试液不变色 取反应后溶液适量于试管中,滴加石蕊试液 石蕊试液变红色 不正确 氢氧化钠、碳酸钠溶液显碱性,都能使酚酞试液变红色 利用熟石灰改良酸性土壤
【解析】
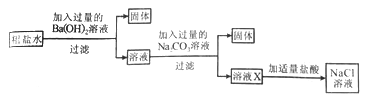
稀盐酸和氢氧化钠反应生成氯化钠和水,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠。
(1)①稀盐酸和氢氧化钠反应生成氯化钠和水,该反应的化学方程式为![]() 。
。
②稀盐酸显酸性,不能使酚酞试液变色,除了“恰好中和”外,还有第二种可能性,这种可能性是稀盐酸过量。
③氢氧化钠和稀盐酸反应生成氯化钠和水,显酸性溶液能使石蕊试液变红色,显中性溶液不能使石蕊试液变色,石蕊试液不变色,说明恰好中和,石蕊试液变红色,说明稀盐酸过量。
实验 | 实验方法 | 实验现象 | 实验结论 |
甲 | 取反应后溶液适量于试管中,滴加石蕊试液 | 石蕊试液不变色 | 恰好中和 |
乙 | 取反应后溶液适量于试管中,滴加石蕊试液 | 石蕊试液变红色 | 第二种可能性 |
(2)碳酸钠溶液显碱性,能使酚酞试液变红色,故不正确,理由是碳酸钠溶液显碱性,能使酚酞试液变红色。
(3)中和反应在实际生产、生活中应用极为广泛,例如利用熟石灰改良酸性土壤。