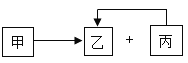题目内容
【题目】某化学兴趣小组的同学要探究铜、X、锌三种金属的活动性顺序,设计了如图所示的实验方案。
![]() 丙试管中观察到的现象是______,反应的化学方程式为______。
丙试管中观察到的现象是______,反应的化学方程式为______。

![]() 若乙试管中无现象,则三种金属的活动性弱到强的顺序是______。
若乙试管中无现象,则三种金属的活动性弱到强的顺序是______。
![]() 若甲试管中无现象,则______试管的实验是多余的。去掉多余的实验,同学们将另两支试管中反应后的物质倒入同一大烧杯中,一段时间后过滤,得到不溶物取不溶物于试管丁中,加入过量稀硫酸,发现有气泡产生,则不溶物中一定含有______,试管丁中一定含有的可溶性物质是______。
若甲试管中无现象,则______试管的实验是多余的。去掉多余的实验,同学们将另两支试管中反应后的物质倒入同一大烧杯中,一段时间后过滤,得到不溶物取不溶物于试管丁中,加入过量稀硫酸,发现有气泡产生,则不溶物中一定含有______,试管丁中一定含有的可溶性物质是______。
【答案】出现红色固体,溶液由蓝色变成无色 ![]() X、铜、锌 乙 铜和锌 硫酸和硫酸锌
X、铜、锌 乙 铜和锌 硫酸和硫酸锌
【解析】
解:![]() 丙试管中锌与硫酸铜反应生成了铜和硫酸锌,观察到的现象是出现红色固体,溶液由蓝色变成无色,反应的化学方程式为
丙试管中锌与硫酸铜反应生成了铜和硫酸锌,观察到的现象是出现红色固体,溶液由蓝色变成无色,反应的化学方程式为![]() 。
。
![]() 若乙试管中无现象,说明了X的活动性小于铜,由丙可知,铜的活动性小于锌,则三种金属的活动性弱到强的顺序是X、铜、锌。
若乙试管中无现象,说明了X的活动性小于铜,由丙可知,铜的活动性小于锌,则三种金属的活动性弱到强的顺序是X、铜、锌。
![]() 若甲试管中无现象,通过甲、丙即可比较出三种金属的活动性强弱,是
若甲试管中无现象,通过甲、丙即可比较出三种金属的活动性强弱,是![]() 锌
锌![]() 铜,则乙试管的实验是多余的。去掉多余的实验,同学们将另两支试管中反应后的物质倒入同一大烧杯中,一段时间后过滤,得到不溶物取不溶物于试管丁中,加入过量稀硫酸,发现有气泡产生,则不溶物中一定含有铜和锌,试管丁中一定含有的可溶性物质是硫酸和硫酸锌。
铜,则乙试管的实验是多余的。去掉多余的实验,同学们将另两支试管中反应后的物质倒入同一大烧杯中,一段时间后过滤,得到不溶物取不溶物于试管丁中,加入过量稀硫酸,发现有气泡产生,则不溶物中一定含有铜和锌,试管丁中一定含有的可溶性物质是硫酸和硫酸锌。

【题目】某校学习小组准备探究气体的测定和数据处理方法。
(提出问题)
如何利用石灰石(主要成分为CaCO3)与稀盐酸反应来测定生成CO2的质量和体积,并处理数据。
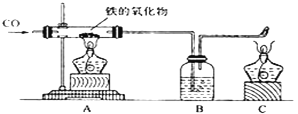
(实验设计)通过下列两个实验分别测定CO2的质量和体积:
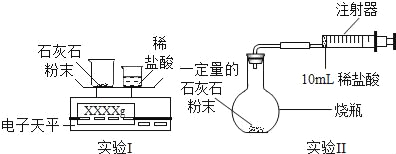
(分析与表达)
(1)上述两个实验中,反应的化学方程式是_____。
(2)实验Ⅰ中,将小烧杯中的所有稀盐酸分几次加入到大烧杯中,并不断搅拌,判断石灰石中CaCO3完全反应的实验现象是_____。
(3)实验Ⅱ中,先连接好装置,再_____(填操作名称),然后装好药品,最后将10ml稀盐酸快速推入烧瓶中。若稀盐酸是缓慢推入的,则可能造成的后果是
_____。
(记录与处理)
(4)已知实验I反应前的总质量[m(大烧杯+石灰石粉末)+m(小烧杯+稀盐酸)],要计算生成CO2的质量,至少还需要的数据是_____。
A m(小烧杯) B m(大烧杯) C m(大烧杯+反应后剩余物)
(5)实验Ⅱ的实验记录如下(表中数据在相同温度、相同压强条件下测定):
时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
注射器读数/ml | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
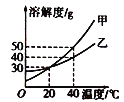
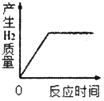
①根据以上实验过程和数据综合分析,最终生成CO2的体积是_____mL,理由是_____。
②根据你的认识,在坐标图中绘制出0~10min生成CO2体积随时间变化的曲线。
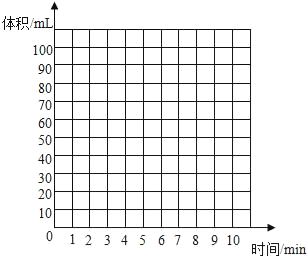
(反思与评价)
(6)经过分析,你认为实验I的优点是_____,实验Ⅱ的优点是_____。