题目内容
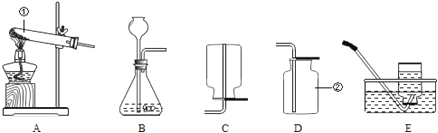
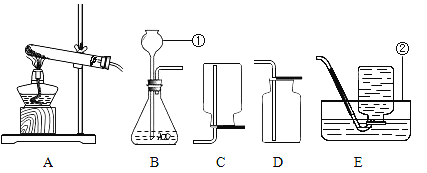
【题目】小亮同学用如图装置测定空气里氧气的含量。试回答下列问题:

(1)实验过程中,燃烧匙里为什么要盛放过量的红磷?_____________
(2)如果反应后进入集气瓶中的水的体积不到总体积的1/5,可能的原因是(写出两条)______
(3)这个实验除了可以得出氧气约占空气体积的1/5外,还可以推断出氮气________(填“易”或“难”)溶于水和其化学性质___________(填“活泼”或“不活泼”)
(4)用碳代替红磷,完成上述实验,发现集气瓶内并没有吸入水,其原因是_________。
【答案】将集气瓶内的氧气充分耗尽 红磷量不足、装置气密性不好、没有冷却到室温就打开了止水夹 难 不活泼 碳与氧气反应生成二氧化碳,虽然消耗了氧气,但又生成了新的气体,集气瓶内压强不变,水不会倒流入集气瓶中
【解析】
(1)为了将集气瓶内的氧气充分耗尽,在做实验时红磷要过量;
(2)如果反应后进入集气瓶中的水的体积不到总体积的1/5,可能的原因是:红磷量不足、装置气密性不好、没有冷却到室温就打开了止水夹;
(3)该实验反应后剩余气体主要是氮气,这个实验除了可以得出氧气约占空气体积的1/5外,还可以推断出氮气难溶于水和其化学性质不活泼;
(4)用碳代替红磷,完成上述实验,发现集气瓶内并没有吸入水,其原因是碳与氧气反应生成二氧化碳,虽然消耗了氧气,但又生成了新的气体,集气瓶内压强不变,水不会倒流入集气瓶中。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】已知某合金粉末除铝外,还含有铁、铜中的一种或两种。某兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究。
(查阅资料)铝与氢氧化钠溶液反应的化学方程式为:![]() ;(产物NaAlO2易溶于水);Fe、Cu不与氢氧化钠溶液反应。
;(产物NaAlO2易溶于水);Fe、Cu不与氢氧化钠溶液反应。
(猜想)猜想1:该合金粉末中除铝外,还含有铁;
猜想2:该合金粉末中除铝外,还含有___________(填名称);
猜想3:该合金粉末中除铝外,还含有铁、铜。
(实验探究)下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液。
实验方案 | 实现现象 | 结论 |
①取一定量的合金粉末,加过量的____________,充分反应后过滤,滤渣备用。 | 粉末部分溶解,并有气泡产生 | 合金中一定含有____________。 |
②取步骤①所得滤渣,加过量的__________,充分反应。 | 滤渣部分溶解,并有气泡产生,溶液呈浅绿色。 | 合金中一定含有___________ |
(探究结论)猜想3成立。
(反思)铝的金属活泼性很强,但常温下却具有很好的抗腐蚀性能,原因是______(用化学方程式表示)