题目内容
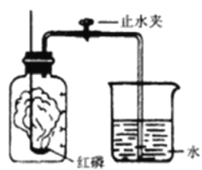
【题目】如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号。

(1)红磷在空气中燃烧的现象是:__________,反应的文字表达式为:___________________。
(2)在实验操作中,当_________________时,打开弹簧夹方能得出较准确结论。
(3)如果实验测量值偏小,可能的原因是:_______________________________。(写一条即可)
【答案】冒白烟红磷+氧气点燃五氧化二磷待红磷熄灭并冷却红磷量不足
【解析】
⑴红磷在空气中燃烧时现象为:剧烈燃烧,产生黄色火焰,生成大量的白烟,故填:冒白烟;红磷+氧气点燃五氧化二磷;⑵在实验操作中,当红磷熄灭,就可以判断瓶内氧气基本消耗完,需要等到冷却后才打开弹簧夹是怕集气瓶内的温度过高,气体膨胀导致瓶内压强比实验后应有的压强要大,使水不能顺着导管升到集气瓶内1/5的高度,导致实验误差较大,所以要等它冷却了才打开弹簧夹;故填:待红磷熄灭并冷却.⑶测量值偏小可能是因为红磷量不足或者弹簧夹没有夹紧,前者是因为不能把氧气全部消耗,后者是因为装置漏气,在等待冷却的过程中会有气体进入,导致测量值偏小,故填:红磷量不足(或弹簧夹没有夹紧)

【题目】(题文)几名同学对蜡烛火焰的焰心进行了以下探究,请你完成其中的一些步骤。
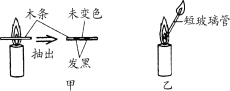
(1)点燃蜡烛,将一根小木条迅速平放入火焰中,约1s后取出,现象如图甲所示,这证明外焰温度最高,你认为原因是__________________。
(2)向焰心处斜向插入一支细短玻璃管,发现玻璃管中无明显现象,在玻璃管的上口点燃,上口产生火焰,如图乙所示,这说明焰心物质的性质是无色。气体具有___________性。
(3)猜想和验证:
(查阅资料)石蜡不完全燃烧时可能产生一氧化碳。常温下,一氧化碳为无色、无味、难溶于水的可燃性气体,燃烧时发出蓝色火焰。
猜想 | 操作 | 现象 | 结论 |
猜想①:焰心气体含有石蜡蒸气 | 取一较长的细玻璃管,用湿冷毛巾包住中部,将玻璃管下端插入焰心,然后再在导管的另一端做点火试验。一段时间后,取下长玻璃管,打开湿毛巾,观察。 | ____________________ | 假设①成立 |
猜想②:焰心气体含有一氧化碳气体 | ________________________________________ | 假设②成立 |
(4)反思:酒精灯的火焰也分为三层,通常用外焰给物质加热,请写出酒精完全燃烧生成
二氧化碳和水的文字表达式:__________________。
【题目】某化学兴趣小组同学在回收废旧电池的同时,开展了如下的实验探究。
(查阅资料)废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水。
(实验1)废干电池的拆卸与处理
(1)兴趣小组同学将废旧干电池卸下的锌筒、碳棒冲洗干净,备用。
(2)将铜帽放入盐酸中,除去锈污,冲洗备用。
(实验2)检验废干电池筒内黑色固体中的二氧化锰存在
兴趣小组同学设计了如下图所示的实验:
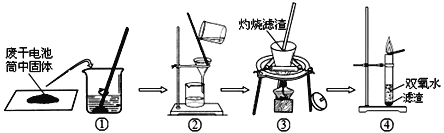
(1)操作③灼烧黑色滤渣时,会产生一种气体能使澄清石灰水变浑浊,灼烧时的表达式为____;澄清石灰水变浑浊的表达式为____。
(2)操作④试管中产生的气体能使带火星木条复燃,该气体为__________。
(3)由此得出结论:滤渣中黑色固体化学式为_____和 _____
(实验3)利用回收锌皮制取氢气及相关探究
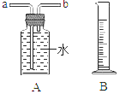
(1)用锌皮和稀硫酸制取氢气。用适当的发生装置,采用排水法收集并测定氢气的体积(如右图),气体从装置A导管口___(填“ a ”或“ b ” ) 进,选用仪器B测量排出水的体积,仪器B名称是______。
(2)探究影响锌与稀硫酸反应快慢的因素。反应过程中用前10 min 内
收集的氢气体积比较反应的快慢。控制其他条件相同,进行下表4组实验,获得数据如下。
实验编号 | 试剂 | 前10 min内产生的 氢气体积(mL) | |
锌的纯度 | 稀硫酸的体积和浓度 | ||
a | 纯锌 | 30 mL 30 % | 564.3 |
b | 含杂质的锌 | 30 mL 30 % | 634.7 |
c | 纯锌 | 30 mL 20 % | 449.3 |
d | 纯锌 | 40 mL 30 % | 602.8 |
[数据分析]
①比较实验a和实验b得到的结论是:_________________________。
②为了研究硫酸浓度对反应快慢的影响,需比较实验____________(填实验编号)。
③探究影响该反应快慢的因素,还需控制的条件是:______________(一例即可)。
(实验4)探究经处理干净的二氧化锰在氯酸钾分解反应中的催化作用(已知氯化钾可溶)
(1)把干燥纯净的24.5g氯酸钾和5.5g二氧化锰混匀、装入大试管中,加热。
(2)待反应完全后,将试管冷却、称量,得到20.4g残留固体。
(3)再将残留固体经溶解、_____、洗涤、干燥、称量,得到5.5g黑色固体。
[数据分析]
①该实验说明:二氧化锰在氯酸钾分解反应前后,_____不变。
②完全反应后制得氧气的质量是______g。(提示:已知所有化学反应遵循如下规律:参加化学反应的各物质的质量总和等于反应后生成各生成物的质量总和)
[实验反思]
要证明二氧化锰是氯酸钾分解反应的催化剂,还要做一个对比实验:将等质量的2份氯酸钾粉末,其中一份加入少量的上述实验所得二氧化锰混匀、装入试管,另一份装入另一试管,加热,比较____________的大小。