��Ŀ����
����Ŀ���ҹ�ҩѧ������������������ű������Чҩ�����أ������ȫ���������˵���������2015��10�»��ŵ����ҽѧ���������о����������ؼ��Ե���������ȡ�����ء����ѵĻ�ѧʽΪC4H10O����ش�
��1��ÿ�����ѷ�������_____��ԭ�ӣ����ѵ���Է�������Ϊ_____��
��2�����ѣ�C4H10O����̼����Ԫ��������Ϊ_____��
��3�����ѣ�C4H10O����̼Ԫ�ص�����������_____����ȷ��0.1%����
���𰸡���1��15��74����2��3��1����3��64.9%
��������
��1�������ѵĻ�ѧʽΪC4H10O��֪��ÿ�����ѷ����к���4��̼ԭ�ӡ�10����ԭ�Ӻ�1����ԭ�ӣ�����15��ԭ�ӣ����ѵ���Է�������=12��4+1��10+16=74��
��2��������̼����Ԫ�ص�������Ϊ��12��4������16��1��=3��1��
��3�����ѣ�C4H10O����̼Ԫ�ص�����������![]() ��100%��64.9%��
��100%��64.9%��

����Ŀ������������������ҽ����е�����ӵȹ�ҵ��ijʵ����ȤС��ӹ����ɼ���Һ����FeSO4������ZnSO4��MgSO4���������������������Ʊ�ʵ�顣
���Ķ����ϣ�
��1��25��ʱ���������������pH��Χ���
Zn��OH��2 | Fe��OH��2 | Mg��OH��2 | |
��ʼ������pH | 5.7 | 7.6 | 10.4 |
������ȫ��pH | 8.0 | 9.6 | 12.4 |
��2��25��ʱ��Zn(OH)2������pH��10.5�ļ���Һ��
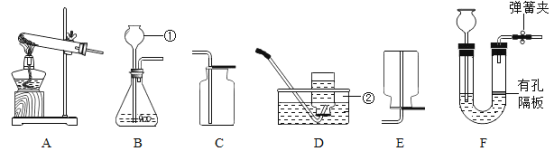
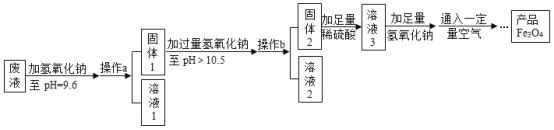
��3���Ʊ�Fe3O4��ʵ���������£�
���ش����⣩
��1������Һ�м�������������Һ���ɳ����Ļ�ѧ����ʽΪ______________��дһ�����ɣ���
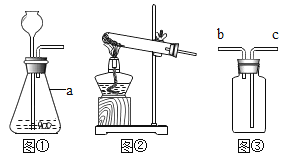
��2������a������Ϊ___���ò�����Ҫ�IJ����������ձ�����������__________�ȡ��������ڴ˲����е���Ҫ������___��
��3����Һ1����������_______������д���֣�����Һ3�������ʵ���Ҫ�ɷ�Ϊ___��