��Ŀ����
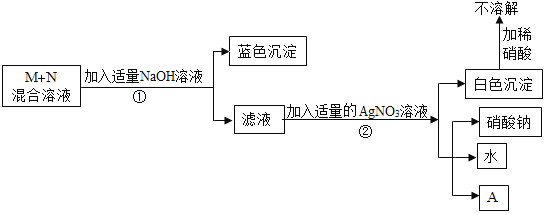
����Ŀ����ͼ�е�����Ϊ���л�ѧ�������ʣ�����֮��ķ�Ӧ��ϵ��ͼ��ʾ(��������ʾת����ϵ����������ʾ��ܷ�Ӧ�����ַ�Ӧ��������Ӧ��������ȥ)������A��Һ��Ӧ�õ�dz��ɫ��Һ��A��B�����кͷ�Ӧ������֮һ�dz����ڳ��õĵ�ζƷ��C�����ڸ���������������C����Һ��D����Һ��Ӧ�ɵõ�B��C����Һ���ҵ���Һ��Ӧ������ɫ�����������������Һ��Ӧ�������ֲ�ͬ��ɫ�ij�������ش�
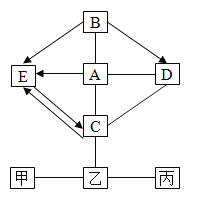
(1)�Ļ�ѧʽ��_____��D�Ļ�ѧʽ��_____��
(2)��ͨ��ʵ������۲�A��B�Ƿ�ǡ����ȫ��Ӧ��ʵ��ǰ��Ҫ��B��Һ�м�����Լ���_____��
(3)E��C��Ӧ�Ļ�ѧ����ʽ��_____��
(4)�����������Һ��Ӧ�Ļ�ѧ����ʽ��_____��
���𰸡�Fe Na2CO3 ��̪��Һ CaO+H2O=Ca(OH)2 CuSO4+Ba(OH)2=Cu(OH)2��+BaSO4��
��������
����A��Һ��Ӧ�õ�dz��ɫ��Һ��A��B�����кͷ�Ӧ������֮һ�dz����ڳ��õĵ�ζƷ����A��B�����кͷ�Ӧ�������Ȼ��ƣ�����ΪA�ͼ�Ӧ����dz��ɫ��Һ������������Ӧ�����Ȼ��������������������������ᷴӦ�����Ȼ��ƺ�ˮ�����A��ϡ���ᣬ��������B���������ƣ��������Ƴ����ڸ����������������C���������ƣ����������ܺ�̼���Ʒ�Ӧ����̼��Ƴ������������ƣ�̼�����ܺ�ϡ���ᷴӦ�����������ܺͶ�����̼��Ӧ����̼���ƣ����D��̼���ƣ�����������Һ���ҵ���Һ��Ӧ������ɫ������˵�����к���ͭ���ӣ������������Һ��Ӧ�������ֲ�ͬ��ɫ�ij������ɴ˿�֪��������ͭ����������������������Ϊ����ͭ������������Ӧ���ɰ�ɫ�������ᱵ����ɫ����������ͭ���������ƺͶ�����̼�ܹ�����ˮ��ϡ������������Ʒ�Ӧ�ܹ�����ˮ���������ƺͶ�����̼��Ӧ�����ܹ�����ˮ�����E��ˮ�������������֤��������ȷ��
�������Ϸ�����֪��
��1���Ļ�ѧʽ��Fe��D�Ļ�ѧʽ��Na2CO3��
��2����ͨ��ʵ������۲�A��B�Ƿ�ǡ����ȫ��Ӧ��ʵ��ǰ��Ҫ��B��Һ�м�����Լ��Ƿ�̪��Һ��������Ϊ����������Һ�м����̪��Һʱ����Һ���ɫ������ϡ����ĵμӣ��������ƺ�ϡ���ᷴӦ������ɫ�ո���ʧʱ��˵���������ƺ�ϡ����ǡ����ȫ��Ӧ��
��3��ˮ�ܺ������Ʒ�Ӧ�����������ƣ���Ӧ�Ļ�ѧ����ʽΪ��CaO+H2O=Ca(OH)2��
��4������ͭ������������Ӧ���ɰ�ɫ�������ᱵ����ɫ����������ͭ����Ӧ�Ļ�ѧ����ʽΪ��CuSO4+Ba(OH)2=Cu(OH)2��+BaSO4����