题目内容
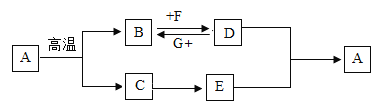
【题目】如图是从两种含铜的废弃物中回收金属铜和硫酸亚铁晶体的方法,请回答下列问题:

(1)氧化铜与稀硫酸反应的现象为________;
(2)写出铁与硫酸铜溶液反应的化学方程式:________,此反应的基本反应类型为________;
(3)固体B中还含有氧化铜,请从实验操作角度分析可能的两个原因:________;________.
(4)操作b为蒸发浓缩、冷却结晶、过滤,蒸发过程中用到的玻璃仪器为________.
【答案】黑色固体逐渐溶解,溶液由无色变成蓝色 Fe+CuSO4═FeSO4+Cu 置换反应 氧化铜没有完全反应 没有冷却至室温就停止通氢气,导致部分铜被氧气氧化 玻璃棒
【解析】
(1)氧化铜与稀硫酸反应生成硫酸铜和水,反应过程中黑色固体逐渐溶解,溶液由无色变成蓝色.故填:黑色固体逐渐溶解,溶液由无色变成蓝色;
(2)铁和硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu,该反应是单质与化合物反应生成单质与化合物,属于置换反应。故填:Fe+CuSO4═FeSO4+Cu;置换反应;
(3)固体B中还含有氧化铜,从实验操作角度分析可能的两个原因是:氧化铜没有完全反应,没有冷却至室温就停止通氢气,导致部分铜被氧气氧化。故填:氧化铜没有完全反应;没有冷却至室温就停止通氢气,导致部分铜被氧气氧化;
(4)蒸发过程中用到的玻璃仪器是玻璃棒,玻璃棒的作用是搅拌使液体均匀受热,防止液体飞溅。故填:玻璃棒。

练习册系列答案
相关题目