题目内容
【题目】某气体由CH4、C3H4、C3H6中的一种或几种组成,取该气体样品在氧气中完全燃烧,测得生成的二氧化碳和水的质量比为22∶9,下列对该气体组成判断正确的是
A.该气体可能是CH4和C3H4 B.该气体中一定没有C3H4
C.该气体可能是CH4和C3H6 D.该气体不可能是C3H6
【答案】A
【解析】
试题分析:根据生成的二氧化碳和水的质量比为22∶9,说明生成的二氧化碳和水的分子个数比为1:1,进一步判断气体中的碳、氢原子个数比为1:2,故根据“中间取值法”的思想,该气体的可能组成为:1、该气体可能是C3H6,2、CH4和C3H4的混合物,3、CH4、C3H6和C3H4的混合物,故选A

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
【题目】实验室部分装置如A-E图所示。
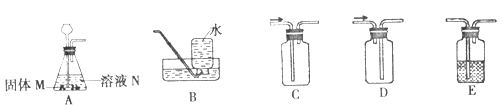
请回答下列问题:
(1)用所给装置制取并收集不同气体,填写下表空白。
固体M | 溶液N | 制取的气体 | 收集装置 |
大理石 | _____① _______ | CO2 | _____② ______ |
____③ ______ | 过氧化氢溶液 | O2 | ____④ ____或C |
锌粒 | 稀硫酸 | ____⑤ ____ | B或____⑥ ____ |
(2)收集干燥的CO2还需要用装置E,E中盛装的试剂为_______⑦ ______。
(3)用上图装置A制取O2时发生反应的化学方程式为________⑧ ________。